
 .
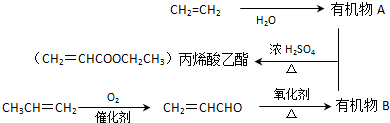
. 分析 CH2=CH2和水發生加成反應,生成A為CH3CH2OH,CH2=CHCHO發生氧化反應生成B為CH2=CHCOOH,CH2=CHCOOH與CH3CH2OH發生酯化反應生成丙烯酸乙酯,根據官能團的性質和變化判斷反應類型并寫出反應的化學方程式.
解答 解:CH2=CH2和水發生加成反應,生成A為CH3CH2OH,CH2=CHCHO發生氧化反應生成B為CH2=CHCOOH,CH2=CHCOOH與CH3CH2OH發生酯化反應生成丙烯酸乙酯,
(1)丙烯醛(CH2=CHCHO)中含有的官能團有碳碳雙鍵、醛基,故答案為:碳碳雙鍵、醛基;
(2)CH2=CHCOOH與CH3CH2OH發生酯化反應生成丙烯酸乙酯,也為取代反應,反應的方程式為CH2=CHCOOH+CH3CH2OH$?_{△}^{濃硫酸}$CH2=CHCOOCH2CH3+H2O,
故答案為:CH2=CHCOOH+CH3CH2OH$?_{△}^{濃硫酸}$CH2=CHCOOCH2CH3+H2O;
(3)CH2=CHCH3含有C=C,可發生加聚反應,反應的方程式為nCH2=CHCH3$\stackrel{引發劑}{→}$ ,
,
故答案為:nCH2=CHCH3$\stackrel{引發劑}{→}$ .
.
點評 本題考查有機物的合成,題目難度不大,本題注意把握常見有機物的官能團的性質,記住反應條件,常見有機物反應的化學方程式要會寫.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題

| A. | 視黃醛的分子式為C21H26O | |
| B. | 維生素A分子結構中含有苯環、碳碳雙鍵和羥基 | |
| C. | 視黃醛是維生素A的氧化產物 | |
| D. | 1 mol甲和1 mol乙在一定條件下均最多能與6 mol H2發生反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
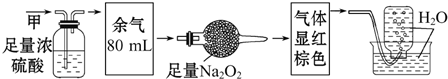
| A. | NH3、NO2、N2 | B. | NH3、NO、CO2 | C. | NH3、NO2、CO2 | D. | NO、CO2、N2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 燒杯①中,若構成微型電池,負極反應式為2Al-6e-=2Al3+,正極反應式為 6H++6e-=3H2↑ | |
| B. | 燒杯①中,若將電解質溶液換成濃硝酸,構成微型電池時鋁為負極,銅為正極 | |
| C. | 燒杯②中,若鐵、銅構成微型電池,則鐵為負極;若鋁、鐵構成微型電池,則鐵為正極 | |
| D. | 燒杯②中,固體最終完全溶解,溶液呈藍色.向溶液中滴加KSCN溶液,溶液不變色 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
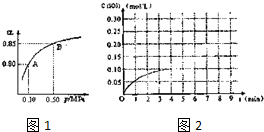
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

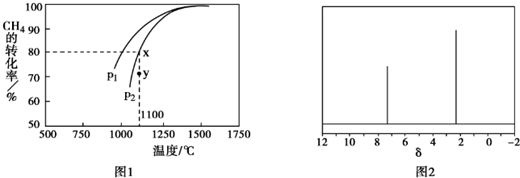
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com