
| A. | ①② | B. | ②⑤ | C. | ③④ | D. | ④⑥ |
分析 ①生成物質量增大小于混合物總質量增大,生成物的質量分數可能降低;
②平衡向正反應移動,生成物的產量一定增加;
③增大某一反應的濃度,平衡向正反應移動,其它反應物的轉化率增大,自身轉化率降低;
④如增大反應物的濃度,平衡向正方向移動,達到平衡時,反應物的濃度比改變條件前大;
⑤平衡向正反應移動,正反應速率一定大于逆反應速率;
⑥加入催化劑,正逆反應速率同等程度增大,平衡不移動.
解答 解:①總質量不變,向正反應移動,生成物的質量分數一定增大,若生成物質量增大小于混合物總質量增大,生成物的質量分數可能降低,故①錯誤;
②平衡向正反應移動,生成物會增加,即生成物的產量一定增加,故②正確;
③降低生成物的濃度,平衡向正反應方向移動,反應物的轉化率一定增大,但增大某一反應的濃度,平衡向正反應移動,其它反應物的轉化率增大,自身轉化率降低,故③錯誤;
④如增大反應物的濃度,平衡向正方向移動,達到平衡時,反應物的濃度比改變條件前大,故④錯誤;
⑤平衡向正反應移動,正反應速率一定大于逆反應速率,故⑤正確;
⑥加入催化劑,正逆反應速率同等程度增大,平衡不移動,故⑥錯誤;
綜上所述②⑤正確,
故選B.
點評 本題考查化學平衡的影響因素,題目難度中等,注意影響化學平衡移動的因素,解答時注意從勒沙特列原理的角度分析,側重于考查學生的分析能力.


科目:高中化學 來源: 題型:選擇題
| A. | 石油、沼氣、天然氣、植物油都屬于可再生能源 | |
| B. | 應用蓋斯定律,可計算某些難以直接測量的反應焓變 | |
| C. | 水蒸氣變為液態水時放出的能量就是該變化的反應熱 | |
| D. | 同溫同壓下,H2(g)+Cl2(g)═2HCl(g)在光照和點燃條件下的△H不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放電時Pb極為負極 | |
| B. | 充電時蓄電池上標有“+”號電極連接電源正極 | |
| C. | 放電時正極反應為PbO2+SO42-+4H++2e═PbSO4+2H2O | |
| D. | 充電時蓄電池上標有“-”號的電極發生氧化反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中:c(OH-)>c(Na+)>c(CO32-)>c(HCO3-)>c(H+) | |
| B. | 該溶液中:c(Na+)+c(H+)═c(OH-)+2c(CO32-)+c(HCO3-) | |
| C. | 加水稀釋該溶液,恢復至原溫度,pH增大,Kw不變 | |
| D. | 該溶液pH約為13的原因:CO32-+H2O═HCO3-+OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 加水稀釋后所有的離子濃度均減小 | |
| B. | 與等體積等濃度的鹽酸反應后,有:c(NH3.H2O)+c(OH-)=c(H+) | |
| C. | 加入等濃度的鹽酸到pH=7時,有:c(NH4+)+c(NH3.H2O)=c(Cl-) | |
| D. | 該溶液在與鹽酸完全中和的過程中,H2O的電離度不斷增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 摩爾是一種物理量 | |
| B. | 溶液中或熔融狀態下能導電的物質就是電解質 | |
| C. | 氧化還原反應的本質是元素化合價發生了變化 | |
| D. | 得電子的物質被還原,是氧化劑 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
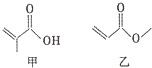
| A. | 甲、乙互為同分異構體 | |
| B. | 甲、乙都能與溴的單質發生加成反應 | |
| C. | 一定條件下,甲、乙均能發生取代反應 | |
| D. | 甲、乙都能與金屬鈉反應生成氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該溶液中存在兩個平衡、七種粒子 | |
| B. | 該溶液中K+、NH4+、NO3-、Al3+可以大量共存 | |
| C. | 滴加少量稀硫酸,充分振蕩無現象 | |
| D. | 通入足量SO2氣體,發生反應的離子方程式:2S2-+SO2+2H2O═3S↓+4OH- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com