
| A. | 16:9 | B. | 23:9 | C. | 1:2 | D. | 2:1 |
分析 首先根據化學方程式和已知條件“R和M的相對分子質量之比為22:9”以及R的質量,列出比例式,即可求出M的質量;
然后根據質量守恒定律,在化學反應中,參加反應前各物質的質量總和等于反應后生成各物質的質量總和,則Y的質量=R的質量+M的質量-X的質量;然后寫出兩者的比,據此選擇即可.
解答 解:根據已知條件“R和M的相對分子質量之比為22:9”,則R:2M=22:2×9=22:18,
設生成的M的質量為a,則22:18=4.4g:a,解之得:a=3.6g;
再根據質量守恒定律可得Y的質量=4.4g+3.6g-1.6g=6.4g;
所以此反應中Y和M的質量比是6.4g:3.6g=16:9,
故選:A.
點評 本題主要考查學生運用化學方程式和質量守恒定律解答實際問題的能力.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:實驗題
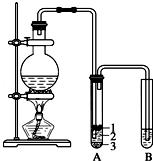 實驗室制取少量溴乙烷的裝置如圖所示.根據題意完成下列填空:
實驗室制取少量溴乙烷的裝置如圖所示.根據題意完成下列填空:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 編號 | 電極材料 | 電解質溶液 | 電子流向 |
| ① | Mg-Al | HNO3(濃) | Mg→Al |
| ② | Mg-Al | HCl(aq) | Mg→Al |
| ③ | Mg-Al | NaOH(aq) | Al→Mg |
| ④ | Al-Cu | HNO3(濃) | Cu→Al |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 無色溶液:Al3+、NH4+、Cl-、HCO3- | |
| B. | 使紫色石蕊試紙變紅色的溶液:Cl-、NO3-、Fe2+、K+ | |
| C. | 常溫下,pH=13的溶液:K+、CO32-、Na+ | |
| D. | c(H+)=0.1mol/L的溶液:CO32-、Na+、HCO3-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 兩溶液一定是等體積混合 | B. | 溶液中:c(R2-)+c(HR-)+c(OH-)=c(Na+)+c(H+) | ||
| C. | 溶液中2c(R2-)+c(HR-)=c(Na+) | D. | 溶液中:c(HR-)>c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 95g | B. | 10g | C. | 50g | D. | 100g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ⑤ | |||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
| 4 | ⑪ | ⑫ |
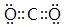 ;元素⑥可形成一種堿性氧化物,用電子式表示該堿性氧化物的形成過程
;元素⑥可形成一種堿性氧化物,用電子式表示該堿性氧化物的形成過程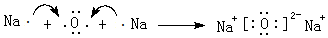 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 測定溶液的pH值,應先將pH試紙用蒸餾水潤濕 | |
| B. | 稱量加熱后的固體時,均需先將固體在空氣中冷卻后再稱量 | |
| C. | 配制0.1mol/LNa2CO3溶液時,容量瓶應先用0.1mol/L Na2CO3潤洗 | |
| D. | 除去鐵粉中混有的少量鋁粉,可加人過量的氫氧化鈉溶液,完全反應后過濾、干燥 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

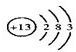 ; F的化學式FeCl2.
; F的化學式FeCl2.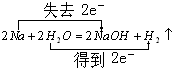 .反應②:
.反應②: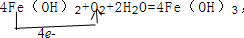 .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com