

 ; F的化學式FeCl2.
; F的化學式FeCl2.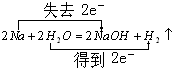 .反應②:
.反應②: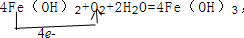 .
. 分析 甲、乙、丙為三種金屬單質;A、C、D常溫下為氣體,其中C呈黃綠色判斷為Cl2;G為白色沉淀;H為紅褐色沉淀判斷為Fe(OH)3;G為Fe(OH)2,B溶液焰色反應顯黃色說明含有鈉元素,金屬甲和水反應生成氣體A和堿B,金屬乙和堿反應證明為Al,所以B為NaOH,甲為Na,A為H2,D為HCl,E為鹽酸溶液,依據G的成分可知F一定含鐵元素,因此丙為Fe,金屬鐵和鹽酸溶液反應生成F為FeCl2,依據判斷出的物質分析回答問題.
解答 解:甲、乙、丙為三種金屬單質;A、C、D常溫下為氣體,其中C呈黃綠色判斷為Cl2;G為白色沉淀;H為紅褐色沉淀判斷為Fe(OH)3;G為Fe(OH)2,B溶液焰色反應顯黃色說明含有鈉元素,金屬甲和水反應生成氣體A和堿B,金屬乙和堿反應證明為Al,所以B為NaOH,甲為Na,A為H2,D為HCl,E為鹽酸溶液,依據G的成分可知F一定含鐵元素,因此丙為Fe,金屬鐵和鹽酸溶液反應生成F為FeCl2;
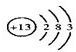
(1)已知甲原子的質量數為23,甲為Na,原子的質子數為11,依據質子數+中子數=質量數;則原子核內的中子數為12;
故答案為:12;
(2)乙元素為鋁元素,原子的結構示意圖為: ,上述推斷可知,F為氯化亞鐵的化學式為:FeCl2;
,上述推斷可知,F為氯化亞鐵的化學式為:FeCl2;
故答案為: ;FeCl2;
;FeCl2;
(4)B為NaOH與乙為Al反應生成A為H2,反應的離子反應方程式為:2Al+2OH-+2H2O=2AlO2-+3H2↑;
故答案為:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(5)反應①是鈉和水反應生成氫氧化鈉和氫氣的反應,鈉失電子水中的氫元素原子得到電子,依據反應電子守恒,化學反應方程式中標出電子轉移的方向與總數為: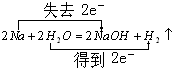 ,反應②為Fe(OH)2,被空氣中的氧氣氧化成氧化鐵,反應的化學反應方程式并標出電子轉移的方向與總數為
,反應②為Fe(OH)2,被空氣中的氧氣氧化成氧化鐵,反應的化學反應方程式并標出電子轉移的方向與總數為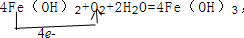 ,
,
故答案為: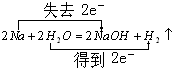 ;
;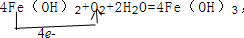 .
.
點評 本題考查了物質轉化關系的分析應用,物質性質的綜合應用,主要是質量數計算應用,原子結構示意圖,氧化還原反應的電子轉移方向和數目,反應條件、反應現象和物質的物理性質是判斷的依據,難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 16:9 | B. | 23:9 | C. | 1:2 | D. | 2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
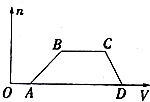 某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的幾種物質,往該溶液中逐漸加入NaOH溶液,產生沉淀的物質的量(n)與加入的NaOH溶液體積(V)的關系如圖所示.回答下列問題:
某混合溶液中可能含有H2SO4、MgCl2、Al2(SO4)3、NH4Cl、NaCl中的幾種物質,往該溶液中逐漸加入NaOH溶液,產生沉淀的物質的量(n)與加入的NaOH溶液體積(V)的關系如圖所示.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH4、C2H4、C3H4 | B. | C2H6、C3H6、C4H6 | C. | CH4、C2H6、C3H8 | D. | C2H4、C2H6、C3H4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
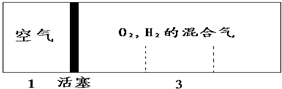
| A. | 2:7 | B. | 5:4 | C. | 1:1 | D. | 7:2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cu$→_{△}^{O_{2}}$CuO$\stackrel{H_{2}O}{→}$Cu(OH)2 | |
| B. | Fe2O3$\stackrel{鹽酸}{→}$FeCl3溶液$\stackrel{NaOH、過濾、加熱}{→}$Fe2O3 | |
| C. | Mg(OH)2$\stackrel{鹽酸}{→}$MgCl2(aq)$\stackrel{電解}{→}$Mg | |
| D. | Na$→_{△}^{O_{2}}$Na2O$\stackrel{CO_{2}}{→}$Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 物質 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸點/℃ | 64.7 | 249 | 199.6 |
 C6H5COOCH3+H218O.
C6H5COOCH3+H218O.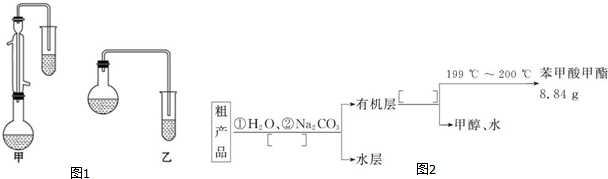
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com