
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅤⅡ | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | ⑪ | ⑫ |
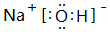 ,該物質和⑤的最高價氧化物對應水化物發生反應的化學反應方程式是NaOH+Al(OH)3=NaAlO2+2H2O
,該物質和⑤的最高價氧化物對應水化物發生反應的化學反應方程式是NaOH+Al(OH)3=NaAlO2+2H2O分析 由元素在周期表中位置,可知①為N、②為F、③為Na、④為Mg、⑤為Al、⑥為Si、⑦為S、⑧為Cl、⑨為Ar、⑩為K、⑪為Ca、⑫為Br.
(1)同周期自左而右金屬性減弱、非金屬性增強,同主族自上而下金屬性增強、非金屬性減弱;
稀有氣體原子最外層為穩定結構,化學性質最不活潑;
同周期自左而右原子半徑減小、同主族自上而下原子半徑增大;
(2)所有元素的最高價氧化物對應的水化物中酸性最強的是高氯酸,K的金屬性最強,故氫氧化鉀的堿性最強;
(3)③的最高價氧化物對應水化物為NaOH,⑤的最高價氧化物對應水化物Al(OH)3,二者反應生成偏鋁酸鈉與水;
(4)可以根據金屬與水或酸反應難易程度、劇烈程度,或者最高價氧化物對應水化物堿性強弱、金屬之間相互置換等進行判斷.
解答 解:由元素在周期表中位置,可知①為N、②為F、③為Na、④為Mg、⑤為Al、⑥為Si、⑦為S、⑧為Cl、⑨為Ar、⑩為K、⑪為Ca、⑫為Br.
(1)同周期自左而右金屬性減弱、非金屬性增強,同主族自上而下金屬性增強、非金屬性減弱,故上述元素中看K的金屬性最強,F的非金屬性最強,稀有氣體Ar原子最外層為穩定結構,化學性質最不活潑,同周期自左而右原子半徑減小、同主族自上而下原子半徑增大,故K原子半徑最大,
故答案為:K;F;Ar;K;
(2)所有元素的最高價氧化物對應的水化物中酸性最強的是HClO4,K的金屬性最強,故氫氧化鉀的堿性最強,
故答案為:HClO4;KOH;
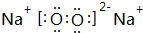
(3)③的最高價氧化物對應水化物為NaOH,電子式為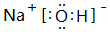 ⑤的最高價氧化物對應水化物Al(OH)3,二者反應生成偏鋁酸鈉與水,化學反應方程式為:NaOH+Al(OH)3=NaAlO2+2H2O,
⑤的最高價氧化物對應水化物Al(OH)3,二者反應生成偏鋁酸鈉與水,化學反應方程式為:NaOH+Al(OH)3=NaAlO2+2H2O,
故答案為: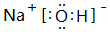 ;NaOH+Al(OH)3=NaAlO2+2H2O;
;NaOH+Al(OH)3=NaAlO2+2H2O;
(4)NaOH溶液堿性比Mg(OH)2強等,可以說明Na的金屬性比Mg的強,
故答案為:NaOH溶液堿性比Mg(OH)2強.
點評 本題考查元素周期表與元素周期律應用,理解掌握元素周期律的應用,掌握金屬性、非金屬性強弱比較實驗事實.


 鷹派教輔銜接教材河北教育出版社系列答案
鷹派教輔銜接教材河北教育出版社系列答案 初中暑期銜接系列答案
初中暑期銜接系列答案科目:高中化學 來源: 題型:解答題
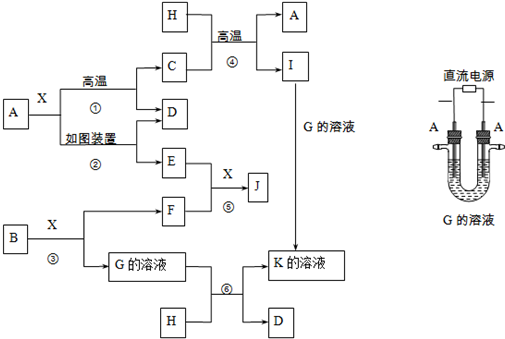
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | “西氣東輸”中的“氣”主要成分是甲烷 | |
| B. | 乙烯的結構簡式為CH2CH2 | |
| C. | 分子式為C6H6的物質一定是苯 | |
| D. | 乙烯使溴水褪色說明乙烯與溴發生了取代反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol 鈉與氧氣反應生成 Na2O 或 Na2O2時,失電子數目均為 NA | |
| B. | 1 mol/L 的 NaOH 溶液中含 Na+數目為 NA | |
| C. | 標準狀況下,2.24LC6H6 所含的分子數目為 0.1NA | |
| D. | 1 mol Na2O2 中含有的陰離子數目為 2NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Z的最高價氧化物的水化物能形成多種含Y元素的鹽 | |
| B. | W的氧化物對應水化物的酸性一定強于Z | |
| C. | Y的單質應該保存在水中 | |
| D. | X的氫化物沸點比Z的氫化物沸點低 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①④ | B. | ④ | C. | ②③ | D. | ①③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com