
| A、34S原子核內中子數為16 |
| B、1H216O和1H218O的相對分子質量相差2 |
| C、13C和15N原子的原子序數相差2 |
| D、2H+結合OH-的能力比1H+的更強 |


科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、化學反應分為:離子反應、非離子反應(標準:是否在水溶液中進行) |
| B、分散系分為:溶液、膠體、濁液(標準:分散質粒子的大小) |
| C、化學反應分為:氧化還原反應、非氧化還原反應(標準:元素化合價是否發生變化) |
| D、化合物分為:電解質、非電解質(標準:溶于水或熔融狀態能否導電) |
查看答案和解析>>
科目:高中化學 來源: 題型:
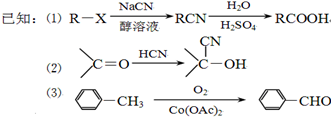
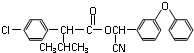 ):
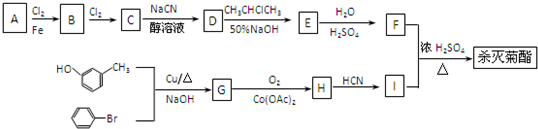
):
| H2O |
| H2SO4 |
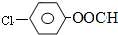 結構,則符合此條件的F共有
結構,則符合此條件的F共有查看答案和解析>>
科目:高中化學 來源: 題型:


 和環狀結構
和環狀結構 是E的最簡單的同系物.
是E的最簡單的同系物.| 濃硫酸 |
| 170℃ |
| Br2 |
查看答案和解析>>
科目:高中化學 來源: 題型:
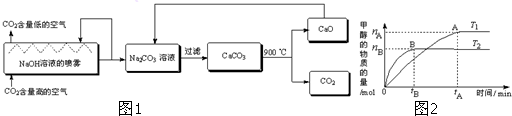
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:


查看答案和解析>>
科目:高中化學 來源: 題型:
| A、1.6 g由氧氣和臭氧組成的混合物中含有氧原子的數目為0.1NA |
| B、0.1 mol H2O中含有電子的數目為NA |
| C、標準狀況下,11.2L四氯化碳中含有分子的數目為0.5NA |
| D、0.5 mol?L-1 CaCl2溶液中的Cl-的數目為NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com