
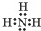 ;NH3在同族元素形成的氫化物中具有較高的沸點,其原因是NH3分子間有氫鍵.
;NH3在同族元素形成的氫化物中具有較高的沸點,其原因是NH3分子間有氫鍵.分析 (1)Al的原子序數為13,含有兩個電子層、最外層含有3個電子,據此判斷在周期表中的位置;同一周期中原子序數越大、原子半徑越小;
(2)該氧化物為氧化鋁,氧化鋁晶體為離子晶體;氧化鋁為兩性氧化物,能夠與氫氧化鈉反應生成偏鋁酸鈉和水;
(3)氨氣為共價化合物,其分子中含有3個氮氫鍵,據此寫出其電子式;氨氣分子中存在氫鍵,導致其沸點較高;
(4)標況下22.4L氨氣的物質的量為1mol,氮元素的最高價氧化物的水化物為硝酸,0.5L 1mol/L的硝酸溶液中含有硝酸的物質的量為:1mol/L×0.5L=0.5mol;1mol氨氣與0.5mol硝酸反應,反應后得到等物質的量的NH3•H2O和NH4NO3的混合溶液,溶液顯堿性,結合電荷守恒判斷離子濃度大小順序;
(5)根據化合價變化判斷,F元素化合價不變,N元素變成NO化合價降低,則另一種物質中的元素化合價只能升高,結合元素組成可知另一種物質為硝酸,據此寫出反應的化學方程式.
解答 解:(1)鋁的核電荷數為13,位于周期表中第三周期IIIA族;鋁的原子序數大于Na,二者處于同一周期,則Al的原子半徑小于鈉,
故答案為:第三周期IIIA族;小;
(2)Al單質在空氣中不易腐蝕,原因是其表面形成了一種致密的且熔點高的化合物氧化鋁,氧化鋁屬于離子晶體;氧化鋁具有兩性,能夠與氫氧化鈉溶液反應生成偏鋁酸鈉和水,反應的離子方程式為:Al2O3+2OH-=2AlO2-+H2O,
故答案為:離子晶體;Al2O3+2OH-=2AlO2-+H2O;
(3)氨氣屬于共價化合物,其電子式為: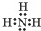 ;氨氣中N的電負性較強,容易形成氫鍵,大大增強了分子間作用力,所以其沸點較高,
;氨氣中N的電負性較強,容易形成氫鍵,大大增強了分子間作用力,所以其沸點較高,
故答案為: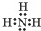 ; NH3分子間有氫鍵;
; NH3分子間有氫鍵;
(4)標況下22.4L氨氣的物質的量為:$\frac{22.4L}{22.4L/mol}$=1mol,
氮元素的最高價氧化物的水化物為硝酸,0.5L 1mol/L的硝酸溶液中含有硝酸的物質的量為:1mol/L×0.5L=0.5mol
1mol氨氣與0.5mol硝酸反應生成0.5mol硝酸銨,還剩余0.5mol一水合氨,
即:反應后得到等物質的量的NH3•H2O和NH4NO3的混合溶液,一水合氨的電離程度大于銨根離子的水解程度,則溶液顯堿性:c(OH-)>c(H+),結合電荷守恒可得:c(NH4+)>c(NO3-),所以溶液中離子濃度大小順序為:c(NH4+)>c(NO3-)>c(OH-)>c(H+),
故答案為:c(NH4+)>c(NO3-)>c(OH-)>c(H+);
(5)NF3是一種新型電子材料,常溫下為穩定氣體,它在潮濕的空氣中與水蒸氣能發生氧化還原反應,其反應的產物有:HF、NO和某種物質,NF3→NO,化合價降低1價,而F元素化合價不變,NF3中N元素的化合價為+3價,根據質量守恒定律可知另一種物質中含有化合價大于+3的N元素,還應該含有H元素,故另一種物質為硝酸,反應的化學方程式為:3NF3+5H2O=9HF+2NO+HNO3,
故答案為:3NF3+5H2O=9HF+2NO+HNO3.
點評 本題考查較綜合,涉及離子濃度大小比較、物質的量濃度的計算、常見化學用語的書寫等知識,題目難度中等,注意掌握原子結構與元素周期律的關系,明確離子濃度大小比較的方法.


科目:高中化學 來源: 題型:選擇題
| A. | 等質量的硫蒸汽和硫固體分別完全燃燒,后者放出的熱量多 | |
| B. | 鍍銅鐵制品鍍層受損后,鐵制品比受損前更容易生銹 | |
| C. | 由C(金剛石)═C(石墨)△H=-1.9 kJ•mol-1可知,金剛石比石墨穩定 | |
| D. | NH3的穩定性強,是因為其分子之間存在氫鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯與溴水(加成反應) | |
| B. | 苯與濃硝酸(取代反應) | |
| C. | 乙醇與乙酸(酯化反應) | |
| D. | 乙醇與氧氣在銅作催化劑下反應(取代反應) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 容器內壓強增大 | B. | KO2的量保持不變 | C. | 平衡常數減小 | D. | 氧氣濃度不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2和H2O | B. | NaCl和HCl | C. | SO2和SiO2 | D. | NaOH和CCl4 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 適宜條件下,SO2和O2可以完全轉化為SO3 | |
| B. | 反應達到平衡后正逆反應的速率皆為零 | |
| C. | 若用18O2進行反應,達到平衡時二氧化硫中也會有18O | |
| D. | 工業合成SO3時,既要考慮反應速率也要考慮反應限度 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下22.4LH20中共價鍵總數為2NA | |
| B. | 32gO3中含有NA個氧原子 | |
| C. | 向裝有催化劑的密閉容器加入1molN2和3 mol H2,充分反應后得2NA個NH3分子 | |
| D. | 1.8g的NH4+中含有電子的物質的量為1mol |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題


 ,它的分子中含有4種不同化學環境的氫原子.
,它的分子中含有4種不同化學環境的氫原子. $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$ +H2O.
+H2O. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com