


 ,它的分子中含有4種不同化學環境的氫原子.
,它的分子中含有4種不同化學環境的氫原子. $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$ +H2O.
+H2O. .
. 分析 A是酒類的主要成分,也可以加入汽油中作為新型燃料,則A為CH3CH2OH,B是最簡單的芳香醛,則B為 ,由反應信息及反應⑤條件可知,F含有醛基,故反應④為乙醇發生催化氧化生成F為CH3CHO,則G為
,由反應信息及反應⑤條件可知,F含有醛基,故反應④為乙醇發生催化氧化生成F為CH3CHO,則G為 ,G發生消去反應生成H為
,G發生消去反應生成H為 ,H發生銀鏡反應、酸化得到I為
,H發生銀鏡反應、酸化得到I為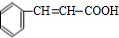 .有機物J(分子式為C20H18O4)是一種果味香精的主要成分,應屬于酯類物質,結合轉化關系可知,乙醇在濃硫酸、加熱條件下發生消去反應生成C為CH2=CH2,乙烯與溴發生加成反應生成D為BrCH2CH2Br,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E為HOCH2CH2OH,結合J的分子式可知,1分子E與2分子I發生酯化反應得到J,故J的結構簡式為:
.有機物J(分子式為C20H18O4)是一種果味香精的主要成分,應屬于酯類物質,結合轉化關系可知,乙醇在濃硫酸、加熱條件下發生消去反應生成C為CH2=CH2,乙烯與溴發生加成反應生成D為BrCH2CH2Br,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E為HOCH2CH2OH,結合J的分子式可知,1分子E與2分子I發生酯化反應得到J,故J的結構簡式為: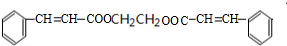 ,據此解答.
,據此解答.
解答 解:A是酒類的主要成分,也可以加入汽油中作為新型燃料,則A為CH3CH2OH,B是最簡單的芳香醛,則B為 ,由反應信息及反應⑤條件可知,F含有醛基,故反應④為乙醇發生催化氧化生成F為CH3CHO,則G為
,由反應信息及反應⑤條件可知,F含有醛基,故反應④為乙醇發生催化氧化生成F為CH3CHO,則G為 ,G發生消去反應生成H為
,G發生消去反應生成H為 ,H發生銀鏡反應、酸化得到I為
,H發生銀鏡反應、酸化得到I為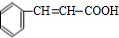 .有機物J(分子式為C20H18O4)是一種果味香精的主要成分,應屬于酯類物質,結合轉化關系可知,乙醇在濃硫酸、加熱條件下發生消去反應生成C為CH2=CH2,乙烯與溴發生加成反應生成D為BrCH2CH2Br,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E為HOCH2CH2OH,結合J的分子式可知,1分子E與2分子I發生酯化反應得到J,故J的結構簡式為:
.有機物J(分子式為C20H18O4)是一種果味香精的主要成分,應屬于酯類物質,結合轉化關系可知,乙醇在濃硫酸、加熱條件下發生消去反應生成C為CH2=CH2,乙烯與溴發生加成反應生成D為BrCH2CH2Br,D在氫氧化鈉水溶液、加熱條件下發生水解反應生成E為HOCH2CH2OH,結合J的分子式可知,1分子E與2分子I發生酯化反應得到J,故J的結構簡式為: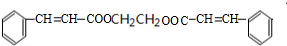 .
.
(1)反應①是乙醇發生消去反應生成乙烯,反應的條件是:濃硫酸、170℃;反應⑧的類型是:酯化反應,
故答案為:濃硫酸、170℃;酯化反應;
(2)B的結構簡式是 ,它的分子中含有4種不同化學環境的氫原子,
,它的分子中含有4種不同化學環境的氫原子,
故答案為: ;4;
;4;
(3)I為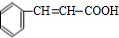 ,分子中所含官能團的名稱是:羧基、碳碳雙鍵,
,分子中所含官能團的名稱是:羧基、碳碳雙鍵,
反應③的化學方程式為:BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2OH+2NaBr,
反應⑥的化學方程式為: $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$ +H2O,
+H2O,
故答案為:羧基、碳碳雙鍵;BrCH2CH2Br+2NaOH$→_{△}^{水}$HOCH2CH2OH+2NaBr; $→_{△}^{濃硫酸}$
$→_{△}^{濃硫酸}$ +H2O;
+H2O;
(5)某有機物K是G( )的同分異構體,同時滿足下列條件:
)的同分異構體,同時滿足下列條件:
Ⅰ.能與FeCl3溶液發生顯色反應,說明含有酚羥基,
Ⅱ.能與溴的四氧化碳溶液發生加成反應,含有碳碳雙鍵;
Ⅲ.苯環上有三個取代基,且有兩個取代基完全相同,含有2個-OH、另外取代基為-CH=CHCH3或-CH2CH=CH2或-C(CH3)=CH2,2個羥基有鄰、間、對3種位置,對應的另一個取代基分別有2、3、1種位置,故符合條件的同分異構體有(2+3+1)×3=18種,
其中一種K的結構中,三個取代基均處于苯環間位上,且其中一個取代基上有支鏈,其結構簡式為 ,
,
故答案為:18; .
.
點評 本題考查有機物的推斷,需要學生對給予的信息進行利用,較好的考查學生自學能力、分析推理能力,明確A與B的結構是推斷關鍵,再結合J的分子式、反應條件進行推斷,需要學生熟練掌握官能團的性質與轉化,(5)中同分異構體數目判斷為易錯點,注意利用定二移一法判斷,難度中等.


 王后雄學案教材完全解讀系列答案
王后雄學案教材完全解讀系列答案科目:高中化學 來源: 題型:解答題
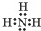 ;NH3在同族元素形成的氫化物中具有較高的沸點,其原因是NH3分子間有氫鍵.
;NH3在同族元素形成的氫化物中具有較高的沸點,其原因是NH3分子間有氫鍵.查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用氨水鑒別Al3+、Mg2+和Ag+ | |
| B. | 用鹽酸、BaCl2溶液鑒別Cl-、SO42-和CO32- | |
| C. | 用溴水鑒別CH4和C2H4 | |
| D. | 用KMnO4酸性溶液鑒別CH3CH2OH和CH3CHO |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
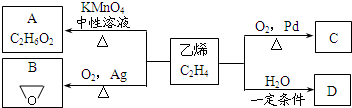 乙烯有如下轉化關系.乙烯在不同的條件下可被氧化成不同產物,如A、B、C.已知:取0.01mol A與足量的鈉完全反應后,生成224mL(標準狀況)氣體.C是B的同分異構體,C與新制的氫氧化銅濁液一起加熱,會產生紅色沉淀.
乙烯有如下轉化關系.乙烯在不同的條件下可被氧化成不同產物,如A、B、C.已知:取0.01mol A與足量的鈉完全反應后,生成224mL(標準狀況)氣體.C是B的同分異構體,C與新制的氫氧化銅濁液一起加熱,會產生紅色沉淀.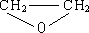 +H2O$\stackrel{一定條件}{→}$
+H2O$\stackrel{一定條件}{→}$ .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
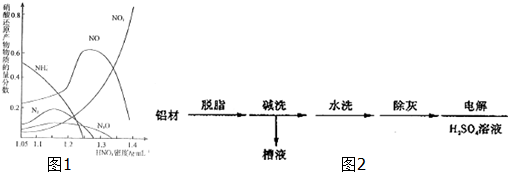
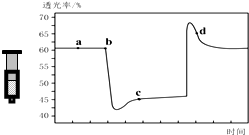 已知反應:2NO2 (紅棕色)?N2O4(無色)△H<0.將一定量的NO2充入注射器中后封口,如圖是在拉伸和壓縮注射器的過程中氣體透光率隨時間的變化(氣體顏色越深,透光率越小).下列說法正確的是( )
已知反應:2NO2 (紅棕色)?N2O4(無色)△H<0.將一定量的NO2充入注射器中后封口,如圖是在拉伸和壓縮注射器的過程中氣體透光率隨時間的變化(氣體顏色越深,透光率越小).下列說法正確的是( )| A. | b點的操作是壓縮注射器 | |
| B. | c點與a點相比,c(NO2)增大,c(N2O4)減小 | |
| C. | d 點:v(正)>v(逆) | |
| D. | 若不忽略體系溫度變化,且沒有能量損失,則T(b)>T(c) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=3的二元弱酸H2R溶液與 pH=11的NaOH溶液混合后,混合液的pH等于7,則混合液中c(R2-)>c(Na+)>c(HR-) | |
| B. | 將0.2 mol/L的某一元弱酸HA溶液和0.1mol/L NaOH溶液等體積混合后溶液中存在:2c(OH-)+c(A-)=2c(H+)+c(HA) | |
| C. | 某物質的水溶液中由水電離出的c(H+)=1×10-amol/L,若a>7,則該溶液的pH為a或14-a | |
| D. | 相同溫度下,0.2mol/L的醋酸溶液與0.1mol/L的醋酸溶液中c(H+)之比小于2:1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com