
分析 (1)根據n=$\frac{n}{m}$計算銅的物質的量,根據n=$\frac{V}{Vm}$計算混合氣體的物質的量,令混合氣體中NO和NO2物質的量分別為xmol、ymol,利用電子轉移守恒、二者物質的量之和列方程,據此計算x、y的值,再根據v=nVm計算NO、NO2的體積;
(2)向反應后溶液中加入NaOH溶液,恰好使溶液中的Cu2+全部轉化成沉淀,此時溶液中溶質為NaNO3,由鈉離子守恒n(NaNO3)=n(NaOH),根據氮原子守恒可知n(HNO3)=n(NaNO3)+n(NO2+NO),再根據c=$\frac{n}{V}$計算;
(3)Cu與硝酸反應得到硝酸銅與NO和NO2混合氣體,NO和NO2混合氣體再在雙氧水、堿性條件下轉化為NaNO3,縱觀整個過程,根據電子轉移守恒,Cu提供的電子等于過氧化氫獲得的電子,據此計算過氧化氫的物質的量,再根據m=nM計算過氧化氫的質量,進而計算需要30%的雙氧水的質量.
解答 解:(1)57.6g銅的物質的量為$\frac{57.6g}{64g/mol}$=0.9mol,22.4L混合氣體的物質的量為$\frac{22.4L}{22.4L/mol}$=1mol,
令混合氣體中NO和NO2物質的量分別為xmol、ymol,
由電子轉移守恒有:3x+y=0.9×2,
由二者物質的量之和:x+y=1,
聯立方程,解得x=0.4,y=0.6,
故NO的體積為0.4mol×22.4L/mol=8.96L,
NO2的體積為0.6mol×22.4L/mol=13.44L,
故答案為:8.96;13.44;
(2)向反應后溶液中加入NaOH溶液,恰好使溶液中的Cu2+全部轉化成沉淀,此時溶液中溶質為NaNO3,由鈉離子守恒n(NaNO3)=n(NaOH)=a V×10 -3mol,根據氮原子守恒可知n(HNO3)=n(NaNO3)+n(NO2+NO)=(a V×10 -3+1)mol,故原有硝酸的物質的量濃度為$\frac{(aV×1{0}^{-3}+1)}{0.2}$mol/L,
故答案為:$\frac{(aV×1{0}^{-3}+1)}{0.2}$;
(3)Cu與硝酸反應得到硝酸銅與NO和NO2混合氣體,NO和NO2混合氣體再在雙氧水、堿性條件下轉化為NaNO3,縱觀整個過程,根據電子轉移守恒,Cu提供的電子等于過氧化氫獲得的電子,銅的物質的量為0.9mol,故Cu提供電子為0.9mol×2=1.8mol,故需要過氧化氫的物質的量為$\frac{1.8mol}{2}$=0.9mol,過氧化氫的質量=0.9mol×34g/mol=30.6g,需要30%的雙氧水的質量為$\frac{30.6g}{30%}$=102g,故答案為:102.
點評 本題考查氧化還原反應的計算,為高頻考點,把握發生的反應及電子、電荷守恒、物質的量的有關計算為解答的關鍵,側重分析與計算能力的考查,題目難度不大.


 沖刺100分單元優化練考卷系列答案
沖刺100分單元優化練考卷系列答案科目:高中化學 來源: 題型:解答題
物質 物質的量/mol 溫度/℃ | NO | H2O |
| T1 | 1.6 | 2.4 |
| T2 | 1.2 | 1.8 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
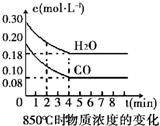 在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O濃度變化如右圖,t℃(高于850℃)時,在相同容器中發生上述反應,容器內各物質的濃度變化如表.
在850℃時發生如下反應:CO(g)+H2O(g)?CO2(g)+H2 (g)△H<0.CO和H2O濃度變化如右圖,t℃(高于850℃)時,在相同容器中發生上述反應,容器內各物質的濃度變化如表.| 時間(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 的敘述中不正確的是( )
的敘述中不正確的是( )| A. | 常溫下,與Na2CO3溶液反應放出CO2 | |
| B. | 能發生水解反應,1 mol 該有機物能與8 mol 的NaOH反應 | |
| C. | 與稀硫酸共熱能生成兩種有機物 | |
| D. | 該物質的化學式是C14H10O9 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、SiO32-、Cl-、NO3- | B. | H+、NH4+、Al3+、SO42- | ||
| C. | Na+、S2-、OH-、SO42- | D. | Na+、C6H5O-、CH3COO-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 酸性氧化物 | 堿性氧化物 | 酸 | 堿 | 強電解質 | 非電解質 | |
| A | NO2 | CuO | HF | KOH | H2SO4 | SO2 |
| B | CO2 | Na2O2 | HCl | Cu(OH)2 | HClO4 | CH4 |
| C | SiO2 | MgO | HClO | NH3•H2O | NaHCO3 | C2H5OH |
| D | Mn2O7 | K2O | HBr | Na2CO3 | Ba(OH)2 | Cl2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 食鹽加碘:著色劑 | B. | 火腿中的NaNO3:防腐劑 | ||
| C. | 炒菜放味精:調味劑 | D. | 用小蘇打發面蒸饅頭:膨松劑 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com