
| A. | 堿性氫氧燃料電池的正極反應:H2-2e-+2OH-═2H2O | |
| B. | 用電子式表示NaCl的形成過程: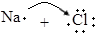 →Na+[ →Na+[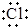 ]- ]- | |
| C. | 少量二氧化硫通入次氯酸鈉堿性溶液中:SO2+C1O一+2OH-═SO42-+Cl-+H2O | |
| D. | 汽車尾氣系統的催化轉化器可降低NO等的排放:2CO+2NO$\frac{\underline{\;催化劑\;}}{\;}$2CO2+N2 |
分析 A.堿性氫氧燃料電池中,負極上失電子發生氧化反應、正極上得電子發生還原反應;
B.Na原子和Cl原子通過得失電子形成離子化合物NaCl;
C.二氧化硫和次氯酸鈉發生氧化還原反應生成硫酸鈉和HCl;
D.在催化劑條件下,CO、NO反應生成二氧化碳和氮氣.
解答 解:A.堿性氫氧燃料電池中,負極上失電子發生氧化反應、正極上得電子發生還原反應,負極反應式為H2-2e-+2OH-═2H2O,故A錯誤;
B.Na原子和Cl原子通過得失電子形成離子化合物NaCl,所以其形成過程為 →Na+[
→Na+[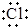 ]-,故B正確;
]-,故B正確;
C.二氧化硫和次氯酸鈉發生氧化還原反應生成硫酸鈉和HCl,離子方程式為SO2+C1O-+2OH-═SO42-+Cl-+H2O,故C正確;
D.在催化劑條件下,CO、NO反應生成二氧化碳和氮氣,從而降低環境污染,反應方程式為:2CO+2NO$\frac{\underline{\;催化劑\;}}{\;}$2CO2+N2,故D正確;
故選A.
點評 本題考查環境污染、氧化還原反應、電子式、電極反應式的書寫等知識點,側重考查基本理論,明確物質的性質是解本題關鍵,注意原電池反應式要結合電解質溶液酸堿性書寫,易錯選項是C.


 世紀百通主體課堂小學課時同步達標系列答案
世紀百通主體課堂小學課時同步達標系列答案 世紀百通優練測系列答案
世紀百通優練測系列答案 百分學生作業本題練王系列答案
百分學生作業本題練王系列答案科目:高中化學 來源: 題型:選擇題
| A. | 常用鋁鹽溶液與氨水反應制取氫氧化鋁 | |
| B. | 澄清石灰水盛裝在用玻璃塞塞緊的試劑瓶中 | |
| C. | 氫氣在氯氣中燃燒產生蒼白色火焰 | |
| D. | 新制氯水通常保存在棕色試劑瓶 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHCO3溶液與鹽酸:CO32-+2 H+=H2O+CO2↑ | |
| B. | 硝酸銀溶液與銅:Cu+Ag+=Cu2++Ag | |
| C. | 金屬鉀與水反應:K+H2O═K++OH-+H2↑ | |
| D. | 用醋酸除水垢:2CH3COOH+CaCO3=Ca2++2CH3COO-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
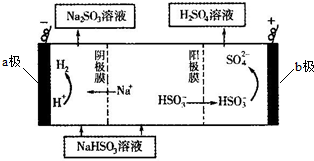
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
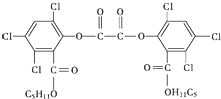 “魔棒”常被用于晚會現場氣氛的渲染.“魔棒”發光原理是利用H2O2氧化草酸二酯產生能量,該能量被傳遞給熒光物質后便發出熒光,草酸二酯(CPPO)結構簡式如圖.下列說法中正確的是( )
“魔棒”常被用于晚會現場氣氛的渲染.“魔棒”發光原理是利用H2O2氧化草酸二酯產生能量,該能量被傳遞給熒光物質后便發出熒光,草酸二酯(CPPO)結構簡式如圖.下列說法中正確的是( )| A. | CPPO難溶于水 | |
| B. | CPPO屬于芳香烴也屬于高分子化合物 | |
| C. | 1 mol CPPO與氫氣完全反應,需要10 mol H2 | |
| D. | 1 mol CPPO與NaOH稀溶液反應(不考慮苯環上氯原子水解),最多消耗4 mol NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | S(s)+O2(g)→SO2(g)+Q1kJ;S(g)+O2(g)→SO2(g)+Q2kJ | |
| B. | H2(g)+$\frac{1}{2}$O2(g)→H2O(l)+Q1kJ;H2(g)+$\frac{1}{2}$O2(g)→H2O(g)+Q2kJ | |
| C. | NaOH(aq)+HCl(aq)→NaCl(aq)+H2O(l)+Q1kJ NaOH(aq)+HAc(aq)→NaAc(aq)+H2O(l)+Q2kJ | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1kJ,H2(g)+I2(g)→2HI(g)+Q2kJ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 反應時間t/s | 1 | 4 | 9 | 16 |
| 鍍層厚度y/nm | a | 2a | 3a | 4a |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學式 | AgCl | Ag2CrO4 | CH3COOH | HClO | H2CO3 |
| Ksp或Ka | Ksp=1.8×10-10 | Ksp=9.0×10-12 | Ka=1.8×10-5 | Ka=3.0×10-8 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
| A. | 相同濃度CH3COONa和NaClO的混合溶液中,各種離子濃度的大小關系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | 次氯酸鈉溶液中通入少量CO2的離子方程式為:2ClO-+CO2+H2O=CO32-+2HClO | |
| C. | 向0.1 mol•L-1CH3COOH溶液中滴加NaOH溶液中至c(CH3COOH):c(CH3COO-)=5:9,此時溶液的pH=5 | |
| D. | 向濃度均為1.0×10-3 mol•L-1的KCl和K2CrO4混合溶液中滴加1.0×10-3 mol•L-1的AgNO3溶液,CrO42-先形成沉淀 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com