

| 反應時間t/s | 1 | 4 | 9 | 16 |
| 鍍層厚度y/nm | a | 2a | 3a | 4a |
分析 (1)化學鍍不需通電;
(2)用熱堿液清洗能除去鍍件表面油污;表面粗化可增大接觸面積;
(3)SnCl2與AgNO3反應生成銀和四氯化錫和硝酸錫;
(4)Ni2+與H2PO2-反應生成鎳、H3PO3及與金屬鎳物質的量相等的氫氣;
(5)鍍層厚度y與反應時間t的關系式為y=at1/2;將鍍層厚度為6anm帶入可得時間;
(6)由c(Ni2+)×c2(OH-)=2.0×10-15計算出c(Ni2+).
解答 解:(1)化學鍍不需通電,電鍍需要通電,故答案為:不需通電;
(2)用熱堿液清洗能除去鍍件表面油污,鍍件表面粗化可增強親水性及增大接觸面積,故答案為:除去鍍件表面油污;增大接觸面積;
(3)SnCl2與AgNO3反應生成銀和四氯化錫和硝酸錫,反應方程式為2SnCl2+4AgNO3═4Ag+SnCl4+Sn(NO3)4,故答案為:2SnCl2+4AgNO3═4Ag+SnCl4+Sn(NO3)4;
(4)Ni2+與H2PO2-反應生成鎳、H3PO3及與金屬鎳物質的量相等的氫氣,反應的離子方程式是2H2O+Ni2++2H2PO2-=Ni++H2↑+2H3PO3,故答案為:2H2O+Ni2++2H2PO2-=Ni++H2↑+2H3PO3;
(5)根據表中數據可可知鍍層厚度y與反應時間t的關系式為y=at1/2;將鍍層厚度為6anm帶入,可知t=36s,故答案為:y=at1/2;36s;
(6)由c(Ni2+)×c2(OH-)=2.0×10-15,c(Ni2+)=$\frac{2.0×10{\;}^{-15}}{(10{\;}^{-4}){\;}^{2}}$mol/L=2×10-7mol/L,即2×10-7mol•L-1×59g•mol-1=1.2×10-5g/L=1.2×10-2mg/L,
故答案為:1.2×10-2.
點評 本題電鍍的制備流程,題目難度中等,本題易錯點為(6),注意單位之間的換算.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:選擇題
| A. | Z可以電離 | B. | Z可以表示為:XY2 | C. | X形成+2價陽離子 | D. | Z的電子式為 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 堿性氫氧燃料電池的正極反應:H2-2e-+2OH-═2H2O | |
| B. | 用電子式表示NaCl的形成過程: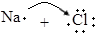 →Na+[ →Na+[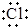 ]- ]- | |
| C. | 少量二氧化硫通入次氯酸鈉堿性溶液中:SO2+C1O一+2OH-═SO42-+Cl-+H2O | |
| D. | 汽車尾氣系統的催化轉化器可降低NO等的排放:2CO+2NO$\frac{\underline{\;催化劑\;}}{\;}$2CO2+N2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙醇、乙酸都可以與鈉反應生成氫氣 | |
| B. | 油脂、淀粉、纖維素都屬于天然高分子化合物 | |
| C. | 甲苯和乙烯都可與溴水發生化學反應造成溴水褪色 | |
| D. | 蛋白質溶液加入CuSO4溶液會析出,這一過程屬于蛋白質的鹽析 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 組分 | CO | CO2 | H2 |
| 體積分數 | 20% | 5% | 75% |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 由圖中信息可知HA為強酸,N點表示酸堿恰好中和 | |
| B. | 常溫下,一定濃度的MA稀溶液的pH<7 | |
| C. | K點所對應的溶液中離子濃度的大小關系:c(M+)>c(OH-)>c(A-)>c(H+) | |
| D. | K點對應的溶液中,溶液的pH>13.c(HA)+c(A-)=0.25mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
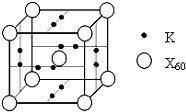 已知X、Y、Z、Q、E五種元素的原子序數依次增大,其中X原子核外電子有6種不同的運動狀態,s能級電子數是p能級電子數的兩倍;Z原子L層上有2對成對電子;Q是第三周期中電負性最大的元素;E的單質是常溫下唯一呈液態的非金屬.請回答下列問題:
已知X、Y、Z、Q、E五種元素的原子序數依次增大,其中X原子核外電子有6種不同的運動狀態,s能級電子數是p能級電子數的兩倍;Z原子L層上有2對成對電子;Q是第三周期中電負性最大的元素;E的單質是常溫下唯一呈液態的非金屬.請回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某研究性學習小組為探究鋅與鹽酸反應,取同質量、同體積的鋅片、同濃度鹽酸做了下列平行實驗:
某研究性學習小組為探究鋅與鹽酸反應,取同質量、同體積的鋅片、同濃度鹽酸做了下列平行實驗:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 是制作電木的原料.下列圍繞此物質的討論正確的是( )
是制作電木的原料.下列圍繞此物質的討論正確的是( )| A. | 該有機物沒有確定的熔點 | B. | 該有機物通過加聚反應得到 | ||
| C. | 該有機物通過苯酚和甲醇反應得到 | D. | 該有機物的單體是-C6H3OHCH2- |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com