
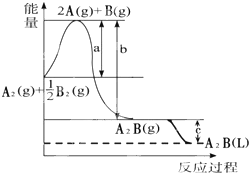
 已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反應過程中能量變化如圖,問:
已知:A2(g)+$\frac{1}{2}$B2(g)═A2B(g),反應過程中能量變化如圖,問:分析 (1)化學反應的實質為舊鍵的斷裂和新鍵的形成,斷裂化學鍵吸收能量,生成化學鍵放出能量,二者的差值是反應的反應熱,不同聚集狀態的物質,能量不同;
(2)反應物與生成物的總能量不同,結合能量守恒判斷反應是吸熱反應還是放熱反應;
(3)由圖象可知A2B吸收能量,結合能量守恒計算.
解答 解:(1)圖象中可以分析判斷,a代表舊鍵斷裂吸收的能量;c為固體和液體之間的能量差,代表A2B由氣態到液態放出的能量,
故答案為:舊鍵斷裂吸收的能量;生成新鍵放出的能量;由氣態到液態放出的能量;
(2)反應物的能量高于生成物的能量,依據化學反應的能量守恒,反應是放熱反應,焓變小于0;
故答案為:放熱;小于零;
(3)由圖象可知A2(g)+$\frac{1}{2}$B2(g)═A2B(g)△H=(a-b)kJ/mol,A2B(g)=A2B(L)△H=-ckJ/mol,則A2B(L)分解的熱化學反應方程式為A2B(L)=A2(g)+$\frac{1}{2}$B2(g)△H=+(b-a+c)kJ/mol,
故答案為:A2B(L)=A2(g)+$\frac{1}{2}$B2(g)△H=+(b-a+c)kJ/mol.
點評 本題考查了化學反應的能量變化,圖象分析判斷,為高頻考點,側重于學生的分析能力的考查,注意把握圖象的分析和識別,把握反應熱△H=反應物能量總和-生成物能量總和,題目較簡單.


科目:高中化學 來源: 題型:解答題
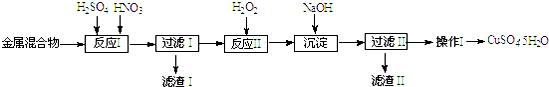
| 陽離子 | Fe3+ | Fe2+ | Cu2+ |
| 開始沉淀 | 1.5 | 6.4 | 4.2 |
| 完全沉淀 | 3.2 | 8.9 | 6.7 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

| 名稱 | 相對分 子質量 | 性狀 | 密度(g/mL) | 沸點(℃) | 溶解性 | |
| 苯胺 | 93 | 無色油狀液體 | 1.02 | 184.4 | 微溶于水 | 易溶于乙醇、乙醚 |
| 乙酸 | 60 | 無色液體 | 1.05 | 118.1 | 易溶于水 | 易溶于乙醇、乙醚 |
| 乙酰 苯胺 | 135 | 白色晶體 | 1.22 | 304 | 微溶于冷水,可溶于熱水 | 易溶于乙醇、乙醚 |
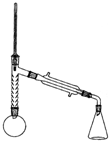
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
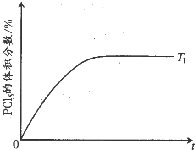
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl5)/mol | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用惰性電極電解NaH2PO2溶液,其陰極反應式為:2H2O-4e-═O2↑+4H+ | |
| B. | H3PO2與過量NaOH溶液反應的離子方程式為:H3PO2+3OH-═PO23-+3H2O | |
| C. | 將H3PO2溶液加入到酸性重鉻酸鉀溶液中,H3PO2的還原產物可能為H3PO4 | |
| D. | H3PO2溶于水的電離方程式為H3PO2?H++H2PO2- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
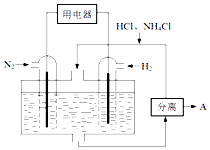 氮及其化合物在工農業生產生活中應用廣泛,請解決下列問題.
氮及其化合物在工農業生產生活中應用廣泛,請解決下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
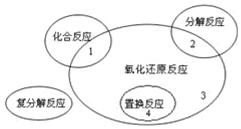
| A. | AgNO3+NaCl═AgCl↓+NaNO3 | B. | 2F2+2H2O═4HF+O2 | ||
| C. | MgCl2(熔融)$\frac{\underline{\;通電\;}}{\;}$Mg+Cl2↑ | D. | 3CO+Fe2O3$\frac{\underline{\;高溫\;}}{\;}$2Fe+3CO2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com