
 ) 發生酯化反應的產物.
) 發生酯化反應的產物. 、
、 、
、 任意一種.
任意一種. ,R-ONa$→_{△}^{Cl-R′}$R-O-R′(R-、R′-表烴基)
,R-ONa$→_{△}^{Cl-R′}$R-O-R′(R-、R′-表烴基)
 .
. 分析 (1)化合物甲與苯氧乙酸( ) 發生酯化反應,則甲中含有羥基;
) 發生酯化反應,則甲中含有羥基;
(2)苯氧乙酸( ) 的同分異構體符合:含有酯基;能與FeCl3溶液發生顯色反應,說明含有酚羥基;且苯環上有2種一硝基取代物,苯環上有2個取代基且處于對位位置,
) 的同分異構體符合:含有酯基;能與FeCl3溶液發生顯色反應,說明含有酚羥基;且苯環上有2種一硝基取代物,苯環上有2個取代基且處于對位位置,
(3)甲蒸氣對氫氣的相對密度是29,則Mr(甲)=29×2=58,5.8g甲的物質的量=$\frac{5.8g}{58g/mol}$=0.1mol,質量守恒可知,參加反應的氧氣的質量=0.3mol×44g/mol+0.3mol×18g/mol-5.8g=12.8g,氧氣物質的量=$\frac{12.8g}{32g/mol}$=0.4mol,根據氧原子守恒,可知5.8g甲中n(O)=0.3mol×2+0.3mol-0.4mol×2=0.1mol,則甲分子中N(C)=$\frac{0.3mol}{0.1mol}$=3、N(H)=$\frac{0.3mol×2}{0.1mol}$=6、N(O)=$\frac{0.1mol}{0.1mol}$=1,故甲的分子式為C3H6O,甲分子中不含甲基,且為鏈狀結構,故甲的結構簡式是CH2=CH-CH2-OH;
(4)苯酚和氫氧化鈉或鈉反應生成苯酚鈉,結合反應信息可知,逆推可知丙是ClCH2COOH,乙為CH3COOH,CH2=CH-CH2-OH和 發生酯化反應生成菠蘿酯為
發生酯化反應生成菠蘿酯為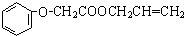 .
.
解答 解:(1)化合物甲與苯氧乙酸( ) 發生酯化反應,則甲中一定含有羥基,
) 發生酯化反應,則甲中一定含有羥基,
故答案為:羥基;
(2)苯氧乙酸( ) 的同分異構體符合:含有酯基;能與FeCl3溶液發生顯色反應,說明含有酚羥基;且苯環上有2種一硝基取代物,苯環上有2個取代基且處于對位位置,所以其同分異構體是:
) 的同分異構體符合:含有酯基;能與FeCl3溶液發生顯色反應,說明含有酚羥基;且苯環上有2種一硝基取代物,苯環上有2個取代基且處于對位位置,所以其同分異構體是: 、
、 、
、 ,
,
故答案為: 、
、 、
、 任意一種;
任意一種;
(3)甲蒸氣對氫氣的相對密度是29,則Mr(甲)=29×2=58,5.8g甲的物質的量=$\frac{5.8g}{58g/mol}$=0.1mol,質量守恒可知,參加反應的氧氣的質量=0.3mol×44g/mol+0.3mol×18g/mol-5.8g=12.8g,氧氣物質的量=$\frac{12.8g}{32g/mol}$=0.4mol,根據氧原子守恒,可知5.8g甲中n(O)=0.3mol×2+0.3mol-0.4mol×2=0.1mol,則甲分子中N(C)=$\frac{0.3mol}{0.1mol}$=3、N(H)=$\frac{0.3mol×2}{0.1mol}$=6、N(O)=$\frac{0.1mol}{0.1mol}$=1,故甲的分子式為C3H6O,甲分子中不含甲基,且為鏈狀結構,故甲的結構簡式是CH2=CH-CH2-OH,
故答案為:CH2=CH-CH2-OH;
(4)苯酚和氫氧化鈉或鈉反應生成苯酚鈉,結合反應信息可知,逆推可知丙是ClCH2COOH,乙為CH3COOH,CH2=CH-CH2-OH和 發生酯化反應生成菠蘿酯為
發生酯化反應生成菠蘿酯為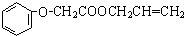 ,
,
①苯酚具有酸性但酸性弱于醋酸、碳酸,所以苯酚能和鈉、氫氧化鈉反應生成苯酚鈉,不能和碳酸氫鈉反應,故選:ac;
②通過以上分析知,其結構簡式為:ClCH2COOH,
故答案為:ClCH2COOH;取代反應;
③在催化劑、加熱條件下,CH2=CH-CH2-OH和 發生酯化反應生成菠蘿酯,反應方程式為
發生酯化反應生成菠蘿酯,反應方程式為 ,
,
故答案為: .
.
點評 本題考查有機物的推斷,需要學生對給予的信息進行利用,較好的考查學生的閱讀能力、自學能力與知識遷移應用能力,題目難度中等,難度中等.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 )所示,回答下列問題.
)所示,回答下列問題.
 .
.
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,B、C、D、E與A形成的化合物中穩定性最強的是H2O(填化學式).
,B、C、D、E與A形成的化合物中穩定性最強的是H2O(填化學式).
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 三者的氧化物均為酸性氧化物 | |
| B. | 三者的單質均存在同素異形現象 | |
| C. | CO2、SiO2、SO3都能與H2O反應,其反應類型相同 | |
| D. | 25℃時,物質的量濃度相同的三溶液的pH:Na2SiO3<Na2SO3<Na2CO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 重結晶法提純苯甲酸時,為了析出更多晶體,熱濾液要用冰鹽水充分冷卻 | |
| B. | 自然界中無游離態的Na、K、Si、Fe,有游離態的S、O | |
| C. | PM2.5是指大氣中直徑小于或等于2.5微米的顆粒物,也稱為“細顆粒物”,PM2.5在空氣中不可能形成膠體 | |
| D. | 硅石、瑪瑙、硅膠的主要成分是二氧化硅 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;取0.2mol/L的NaOH溶液與0.1mol/L的G溶液等體積混合后,加熱至充分反應后,待恢復至室溫,剩余溶液中離子濃度由大到小的順序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此時測得溶液的pH=12,則此條件下G中陰離子的電離平衡常數Ka=4×10-12
;取0.2mol/L的NaOH溶液與0.1mol/L的G溶液等體積混合后,加熱至充分反應后,待恢復至室溫,剩余溶液中離子濃度由大到小的順序是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+),此時測得溶液的pH=12,則此條件下G中陰離子的電離平衡常數Ka=4×10-12查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,該化合物與BA3反應生成B的單質,寫出該反應的化學反應方程式3HClO+2NH3=3HCl+N2+3H2O.
,該化合物與BA3反應生成B的單質,寫出該反應的化學反應方程式3HClO+2NH3=3HCl+N2+3H2O.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 用98%的濃硫酸(密度為1.84g/mL)配制500mL 0.30mol/L稀硫酸的實驗步驟如下:
用98%的濃硫酸(密度為1.84g/mL)配制500mL 0.30mol/L稀硫酸的實驗步驟如下:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com