
 SO2��CO��CO2��NOx�nj��h(hu��n)��Ӱ��^��ĎN���w���������ĺ������ƺ������ǃ�(y��u)���҂�����h(hu��n)������Ч;����
SO2��CO��CO2��NOx�nj��h(hu��n)��Ӱ��^��ĎN���w���������ĺ������ƺ������ǃ�(y��u)���҂�����h(hu��n)������Ч;�������� ��1����ȼ��늳��У�ͨ����������늘O�����O��ͨ��߀ԭ����늘O��ؓ(f��)�O��ԓ����(y��ng)��CԪ�ػ��σr��+2�r׃?y��u)?2�r��HԪ�ػ��σr��0�r׃?y��u)?1�r������CO����������
����A��SO2��B��O2��C��H2SO4��ؓ(f��)�O�϶�������ʧ��Ӻ�ˮ����(y��ng)����������x�Ӻ͚��x�ӣ�
����A��NH3��B��O2��C��HNO3���t���O�l(f��)��߀ԭ����(y��ng)��
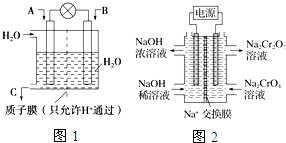
�����x�ӷ������֪��늽⺬��0.02molCuSO4��0.02molNaCl�Ļ����Һ200ml��ꖘO�����x�Ӻ͚������x�ӷ�������Ț�����⣬2Cl--2e-=Cl2����ꎘO���~�x�ӵ���ӣ�
��2������(j��)2CrO42-+2H+?Cr2O72-+H2O�O(sh��)Ӌ�Dʾ�b�ã��������늘O��늽�Na2CrO4��Һ��ȡNa2Cr2O7����Ҫͨ�^늽�늽�����OH-�����Һ�����ԣ��f����ԓ늘O��ꖘO���B���Դ�����O��늘O����(y��ng)ʽ��4OH--4e-�TO2��+2H2O��
��� �⣺��1����ȼ��늳��У�ͨ����������늘O�����O��ͨ��߀ԭ����늘O��ؓ(f��)�O��ԓ����(y��ng)��CԪ�ػ��σr��+2�r׃?y��u)?2�r��HԪ�ػ��σr��0�r׃?y��u)?1�r������CO�����������tͨ��CO��늘O�����O��늘O����ʽ��CO+4 e-+4H+=CH3OH��
�ʴ𰸞飺����CO+4 e-+4H+=CH3OH��
����A��SO2��B��O2��C��H2SO4��ؓ(f��)�O�϶�������ʧ��Ӻ�ˮ����(y��ng)����������x�Ӻ͚��x�ӣ�늘O����(y��ng)ʽ��SO2+2H2O-2e-=SO42-+4H+��
�ʴ𰸞飺SO2+2H2O-2e-=SO42-+4H+��
����A��NH3��B��O2��C��HNO3���t���O�l(f��)��߀ԭ����(y��ng)��������������ˮ��늘O����ʽ��O2+4e-+4H+�T2H2O���ʴ𰸞飺O2+4e-+4H+�T2H2O��
��Ӌ��õ���늽⺬��0.02mol CuSO4��0.02molNaCl�Ļ����Һ200mL����(d��ng)���Ę�(bi��o)�r��0.448L H2�r��n��H2��=$\frac{0.448L}{22.4L/mol}$=0.02mol��
�t�·���D(zhu��n)����0.04mol e-������(j��)늘O����(y��ng)������غ�����Дࣺ
ꖘO��2Cl--2e -=Cl2����
0.02mol 0.02mol 0.01mol
4OH--4e-=2H2O+O2����
0.02mol 0.02mol 0.005mol
ꎘO��Cu2++2e-=Cu
0.02mol 0.02mol
ꖘO�������x�Ӝp��0.02mol���t��Һ�К��x������0.02mol����Һ�К��x�ӝ��=$\frac{0.02mol}{0.2L}$=0.1mol/L����ҺPH=1��
�ʴ𰸞飺Cl2��O2��0.01mol��0.005mol��1��
��2������(j��)2CrO42-+2H+?Cr2O72-+H2O�O(sh��)Ӌ�Dʾ�b�ã��������늘O��늽�Na2CrO4��Һ��ȡNa2Cr2O7����Ҫͨ�^늽�����OH-�������Һ�����ԣ��f����ԓ늘O��ꖘO���B���Դ�����O��늘O����(y��ng)ʽ��4OH--4e-�TO2��+2H2O���ʴ𰸞飺����4OH--4e-�TO2��+2H2O��
�c�u ���}����ԭ늳��O(sh��)Ӌ��ȼ��늳ص�֪�R�c��������(j��)늳ط���(y��ng)ʽ�_����ؓ(f��)�O��늽��|(zh��)���l(f��)����������(y��ng)�Ľ�����ؓ(f��)�O������ؓ(f��)�O���ϻ�Ľ��ٻ�?q��)�늵ķǽ��������O���l(f��)��߀ԭ����(y��ng)��늽��|(zh��)��ԭ늳���늽��|(zh��)�������_����늘O����(y��ng)ʽ����߿����l�c��



| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
| A�� | H2O��H2 | B�� | FeCl3��FeCl2 | C�� | C��CO2 | D�� | CaO��Ca��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
| �x헻����� | A | B | C | D |
| Y | CuO | H2O | SiO2 | FeCl3 |
| W | H2O | Fe3O4 | CO | CuCl2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
| A�� | ����̫��ܵ��坍��Դ���滯ʯȼ�ϣ������ڹ�(ji��)�s�YԴ�����o�h(hu��n)�� | |
| B�� | 늳��е��ؽ��ٵ���Ⱦ���������Ի����������Ԝp����Ⱦ�����o�YԴ | |
| C�� | �˂�?n��i)ճ��������õ����N���W(xu��)Ʒ����(y��ng)�M���p��������ʹ�� | |
| D�� | ���ЙC��܇�ɞ�PM2.5��ֱ����2.5���w���Ҳ�Q�������w����ж����к�����ҪԴ�^����횼��Կ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
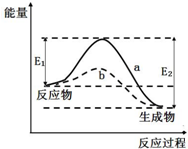
| A�� | ԓ����(y��ng)��H��0 | B�� | a�cb��ȣ�a�ķ���(y��ng)���ʸ��� | ||
| C�� | a�cb��ȣ�����(y��ng)��ƽ�ⳣ��(sh��)Ka=Kb | D�� | ����(y��ng)�ᅡ�I�ܴ��������ᅡ�I�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
| A�� | �^��Ԫ��ȫ���ǽ���Ԫ�� | |
| B�� | ͬ���ڵڢ�A���c�ڢ�A��Ԫ�ص�ԭ����(sh��)��ֵһ����1 | |
| C�� | ����һ���ڽ����c�ǽ��ٵķֽ羀̎���� | |
| D�� | ͬһ����Ԫ�ص�ԭ����(sh��)�IJ���ܞ�10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
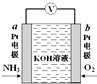 늻��W(xu��)��������������ڱO(ji��n)�y�h(hu��n)����NH3�ĺ������乤��ԭ����D��ʾ��NH3�������鳣Ҋ�o�����|(zh��)�������f���e�`���ǣ�������
늻��W(xu��)��������������ڱO(ji��n)�y�h(hu��n)����NH3�ĺ������乤��ԭ����D��ʾ��NH3�������鳣Ҋ�o�����|(zh��)�������f���e�`���ǣ�������| A�� | ��Һ��OH-��늘Oa�Ƅ� | |
| B�� | ؓ(f��)�O��늘O����(y��ng)ʽ�飺2NH3-6e-+6OH-�TN2��+6H2O | |
| C�� | O2��늘Ob�ϰl(f��)��߀ԭ����(y��ng) | |
| D�� | ����(y��ng)���ĵ�NH3�cO2�����|(zh��)����֮�Ȟ�4��5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ��x���}
| �����ͬF(xi��n)�� | �Y(ji��)Փ | |
| A | ����ˮ�м��������y��Һ���а�ɫ�����a(ch��n)�� | ��ˮ���џoCl2 |
| B | ��SO2ͨ�����Ը��i�����Һ����Һ��ɫ��ȥ | SO2����Ư���� |
| C | ��FeCl3��CuCl2�����Һ�м��������F�ۣ��]�мtɫ���w���� | �����ԣ�Fe3+��Cu2+ |
| D | ��ij��Һ���ȵμ������ữ���ٵμ�BaCl2��Һ���а�ɫ�������� | ԓ��Һ�к���SO42- |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W(xu��) ��Դ�� �}�ͣ�����}
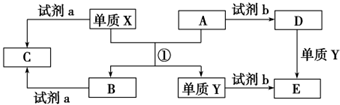
�鿴�𰸺ͽ���>>
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com