
分析 (1)根據公式c=$\frac{n}{V}$,來求硫酸的物質的量濃度;
(2)消耗的硫酸的物質的量是0.012L×18.4mol/L-0.18mol=0.0408mol.設硫酸的還原產物中,硫元素的化合價是n,金屬鋅的物質的量是:$\frac{1.95g}{65g/mol}$=0.03mol,生成硫酸鋅的物質的量是0.03mol,所以0.03mol的硫酸顯示酸性,根據電子守恒和化合價變化之間的關系來計算;
(3)設Fe3O4與Fe2O3物質的量分別為amol,bmol然后鐵守恒和消耗氧氣的量列方程組解;
(4)閃鋅礦(主要成份為ZnS)在空氣中高溫加熱閃鋅礦生成ZnO和SO2,根據固體質量差量法來計算即可,依據硫元素守恒結合反應過程中的定量關系計算得到,反應的關系式為:S~ZnS~SO2~SO3~H2SO4;
解答 解:(1)n(H2SO4)=2n(H2SO4•SO3)=$\frac{445g}{178g/mol}$×2=5mol,所以該硫酸的物質的量濃度為c(H2SO4)=$\frac{5mol}{4.00L}$=1.25mol/L,故答案為:1.25mol/L;
(2)取1.95g鋅加入到12.00mL18.4mol/L的濃硫酸中(反應中只生成一種還原產物),消耗的硫酸的物質的量是0.012L×18.4mol/L-0.18mol=0.0408mol.設硫酸的還原產物中,硫元素的化合價是n,金屬鋅的物質的量是:$\frac{1.95g}{65g/mol}$=0.03mol,生成硫酸鋅的物質的量是0.03mol,所以0.03mol的硫酸顯示酸性,根據電子守恒:$\frac{1.95g}{65g/mol}$×(2-0)=(0.0408mol-0.03mol)×(6-n),解得n=0,所以濃硫酸被還原的產物是硫單質,
故答案為:S;
(3)2934.4L氧氣的物質的量為$\frac{2934.4L}{22.4L/mol}$=131mol,設Fe3O4與Fe2O3物質的量分別為amol,bmol,則3a+2b=48 8a+$\frac{11}{2}$b=131,解得:a=4 b=18,所以Fe3O4物質的量為4mol,Fe2O3物質的量為18mol,
答:反應產物中Fe3O4與Fe2O3物質的量為:Fe3O44 mol,Fe2O3,18 mol;
(4)設ZnS的質量是x,則2ZnS+3O2=2ZnO+2SO2 減少的固體質量
194 161 32
x 1.56-1.32
即$\frac{194}{x}$=$\frac{32}{1.56-1.32}$,解得x=1.455g,
所以ZnS的質量分數=$\frac{1.455}{1.56}$×100%≈93%,
根據S元素守恒,利用關系式發計算,反應的關系式為:S~ZnS~SO2~SO3~H2SO4,
設制得98%的硫酸10t,需要礦石xt
S~ZnS~SO2~SO3~H2SO4
32 98
x×93%×$\frac{32}{97}$(1-2%) 10×98%
x=10.64t
答:樣品中含硫化鋅的質量分數是93%,生產10噸98%的濃硫酸需要這種礦石10.64噸;
點評 本題是一道關于元素以及化合物的計算題,多種解題思想:元素守恒、極限反應的靈活應用是解題的關鍵,難度大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol苯乙烯中含有的碳碳雙鍵數為4NA | |
| B. | 0.1mol甲基中含有的電子數為NA | |
| C. | 2.8 g乙烯和聚乙烯的混合物中所含碳原子數為0.2NA | |
| D. | 標準狀況下,2.24LCHCl3含有的分子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2 | B. | C6H5OH | C. | 裂化汽油 | D. | 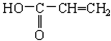 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 紫色石蕊試液中通入二氧化硫,溶液先變紅后褪色 | |
| B. | 將銅片放入濃硫酸中,無明顯現象是因為銅片發生了鈍化 | |
| C. | 硫粉在過量的純氧中燃燒可以生成大量的SO3 | |
| D. | 富含硫黃的礦物在工業上可用于制造硫酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 物質 | 使用的試劑 | 主要操作 |
| A | 乙醇(水) | 金屬鈉 | 過濾 |
| B | 乙酸乙酯(乙酸) | 飽和碳酸鈉溶液 | 振蕩、分液 |
| C | 苯(苯酚) | 濃溴水 | 過濾 |
| D | 乙烷(乙烯) | 酸性高錳酸鉀溶液 | 洗氣 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | +172.22 kJ•mol-1 | B. | -172.22 kJ•mol-1 | ||
| C. | +392.92 kJ•mol-1 | D. | -392.92 kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | COS分子是含有極性鍵的極性分子 | |
| B. | COS的電子式為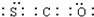 | |
| C. | COS分子中所有原子都滿足8電子穩定結構 | |
| D. | COS屬于離子化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NaHS溶液水解:HS-+H2O?S2-+H3O+ | |
| B. | 向Ca(C1O)2溶液中通入SO2:SO2+2ClO-+H2O=SO32-+2HClO | |
| C. | 硫酸與氫氧化鋇溶液混合:H++SO42-+Ba2++OH-=BaSO4↓+H2O | |
| D. | 向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至SO42ˉ剛好沉淀完全:Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3•H2O+H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com