
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
. 4NO+6H2O.
4NO+6H2O. 分析 據(jù)元素周期表的結構可推出,表中所是元素分別是:①C ②N ③F ④Mg ⑤Al ⑥S ⑦Cl ⑧Ar ⑨K ⑩Br,
(1)最不活潑的元素是稀有氣體,位于元素周期表的0族;
(2)兩性氫氧化物是指既能與酸又能與堿反應,生成鹽與水的物質;
(3)根據(jù)元素性質的遞變規(guī)律,金屬性強的元素位于元素周期表的“左、下”,非金屬性強的元素位于元素周期表的“右、上”.所以金屬性K>Mg>Al,非金屬性C<S<Cl;元素的金屬性越強,其最高價氧化物的水化物的堿性就越強,元素的非金屬性越強,其最高價氧化物的水化物的酸性就越強;
(4)③⑩元素是同主族元素,所以兩者核電荷數(shù)之差是8+18=26;
(5)②元素位于第二周期第ⅤA族,是氮元素,它的氫化物是NH3.
解答 解:根據(jù)元素周期表的結構可推出,表中所是元素分別是:①C ②N ③F ④Mg ⑤Al ⑥S ⑦Cl ⑧Ar ⑨K ⑩Br
(1)最不活潑的元素是稀有氣體,位于元素周期表的0族,是表中的⑧氬元素,其原子結構示意圖為: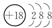 .
.
故答案為: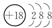 ;
;
(2)表中形成兩性氫氧化物的是Al(OH)3,對應的元素是鋁;⑨元素是鉀,對應的最高價氧化物的水化物是KOH,鋁與氫氧化鉀反應的離子方程式是:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案為:鋁 2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)根據(jù)元素性質的遞變規(guī)律,金屬性強的元素位于元素周期表的“左、下”,非金屬性強的元素位于元素周期表的“右、上”.所以金屬性K>Mg>Al,非金屬性C<S<Cl;元素的金屬性越強,其最高價氧化物的水化物的堿性就越強,元素的非金屬性越強,其最高價氧化物的水化物的酸性就越強,按堿性減弱酸性增強的順序排列是:KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4
故答案為:KOH、Mg(OH)2、Al(OH)3、H2CO3、H2SO4、HClO4;
(4)第三周期有8種元素,第四周期有18種元素,③⑩元素是同主族元素,所以兩者核電荷數(shù)之差是8+18=26.
故答案為:26;
(5)②元素位于第二周期第ⅤA族,是氮元素,它的氫化物是NH3,發(fā)生催化氧化的化學方程式是4NH3+5O2  4NO+6H2O.
4NO+6H2O.
故答案為:4NH3+5O2  4NO+6H2O.
4NO+6H2O.
點評 本題較基礎,需要熟練掌握元素周期表中的1-36號元素的位置與特點,綜合應用元素性質解答此類題目,注意按題目要求作答.


科目:高中化學 來源: 題型:解答題
| 編號 | 實驗操作 | 預期現(xiàn)象和結論 |
| ① | ||
| ② | ||
| ③ | ||
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ;
; ,該六元環(huán)酯的結構簡式為
,該六元環(huán)酯的結構簡式為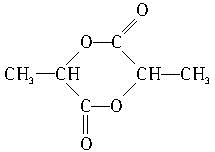 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
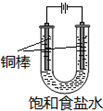 CuCl是應用廣泛的有機合成催化劑,可采取不同方法制取.
CuCl是應用廣泛的有機合成催化劑,可采取不同方法制取. [CuCl3]2-(無色溶液)逆向移動,生成CuCl.
[CuCl3]2-(無色溶液)逆向移動,生成CuCl.查看答案和解析>>
科目:高中化學 來源: 題型:解答題


| 沸點℃ | 密度g/cm3 | 溶解性 | |
| 溴 | 59 | 3.119 | 水中溶解度小,易溶于有機溶劑 |
| 苯 | 80 | 0.8765 | 難溶于水,與有機溶劑互溶 |
| 溴苯 | 156 | 1.50 | 難溶于水,與有機溶劑互溶 |
| 序號 | 實驗步驟 | 預期現(xiàn)象 | 結論 |
| 1 | 將錐形瓶中液體轉入分液漏斗,加入適量四氯化碳,振蕩后分液.分別取少量上層無色溶液于試管A、B中 | ||
| 2 | 錐形瓶中液體含大量 Br- | ||
| 3 | 錐形瓶中液體含大量 H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題

| A. | 按系統(tǒng)命名法命名時,(圖1)化合物的名稱是2,4,6-三甲基-3-乙基庚烷 | |
| B. | 有機物(圖2)的一種芳香族同分異構體能發(fā)生銀鏡反應 | |
| C. | 高分子化合物(圖3),其單體為對苯二甲酸和乙醇 | |
| D. | 前期在西非國家爆發(fā)的埃博拉疫情極具蔓延之勢,已知該病毒對化學藥品敏感.乙醇、次氯酸鈉溶液均可以將病毒氧化而達到消毒的目的 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 15g甲基(-CH3)所含的電子數(shù)為9NA | |
| B. | 300 mL 2 mol/L蔗糖溶液中所含分子數(shù)為0.6 NA | |
| C. | 標準狀況下,22.4LCH4氣體與足量Cl2反應可生成NA個CH3Cl分子 | |
| D. | 80mL 10mol/L濃鹽酸與足量MnO2反應,轉移電子數(shù)為0.4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 元素Y、P的簡單氫化物中化學鍵類型相同 | |
| B. | 原子半徑:X>Y | |
| C. | 最高價氧化物的水化物酸性:P<Q | |
| D. | X、Q兩元素的最高正化合價相同 |
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com