
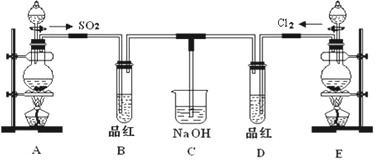
分析 A用于制備SO2,可用Na2SO3與硫酸反應制取,B用于檢驗二氧化硫的生成,E用濃鹽酸和二氧化錳在加熱條件下制備氯氣,D用于檢驗氣體的漂白性,C用于吸收尾氣.
(1)使用分液漏斗時應取下塞子,使分液漏斗內的壓強等于大氣壓強,保證液體順利流出;
(2)實驗室用裝置E制備Cl2,需加熱,為二氧化錳和濃鹽酸的反應,二氧化錳與濃鹽酸在加熱條件下反應生成氯氣和氯化錳、水;生成1mol氯氣,消耗4mol氯化氫,2mol氯化氫顯酸性,2mol氯化氫顯還原性被氧化;
(3)SO2的漂白具有可逆性,次氯酸的漂白不可逆;
(4)氯氣具有較強的氧化性,二氧化硫具有較強的還原性,二氧化硫與氯氣等物質的量反應生成鹽酸和硫酸,鹽酸和硫酸都不具有漂白性.
解答 解:(1)塞子沒有取下來,打開活塞時,空氣無法進入分液漏斗內部,造成分液漏斗內的壓強小于大氣壓強,液體無法流出,使用分液漏斗時應取下塞子,使分液漏斗內的壓強等于大氣壓強,保證液體順利流出,
故答案為:分液漏斗的玻璃塞沒有取下來;
(2)實驗室用裝置E制備Cl2,需加熱,為二氧化錳和濃鹽酸的反應生成氯氣,反應的化學方程式為:MnO2+4HCl(濃)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,離子反應為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑,氯化氫在反應中既表現酸性又表現還原性,4mol氯化氫參加反應,表現為酸性的占$\frac{1}{2}$,若在標準狀態下收集到22.4升的氯氣,物質的量為:$\frac{22.4L}{22.4L/mol}$=1mol,依據方程式可知參加反應的鹽酸有4mol,被氧化的氯化氫為2mol,
故答案為:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++2H2O+Cl2↑;2mol;
(3)次氯酸的漂白性是永久性的,具有不可逆性,二氧化硫的漂白性是暫時的,加熱時,次氯酸漂白過的溶液無變化,二氧化硫和有色物質生成的無色物質不穩定,加熱時會變成紅色,所以B褪色的品紅又恢復成紅色,D無明顯現象,
故答案為:褪色的品紅又恢復成紅色;無明顯現象;SO2漂白后的物質具有不穩定性,加熱時又變成紅色,而氯氣的漂白具有不可逆性;
(4)二氧化硫與氯氣等物質的量反應生成鹽酸和硫酸,鹽酸和硫酸都不具有漂白性,化學方程式為:SO2+Cl2+2H2O=H2SO4+2HCl;
故答案為:SO2+Cl2+2H2O=H2SO4+2HCl.
點評 本題考查氯氣和二氧化硫的漂白性質,題目難度中等,注意掌握氯氣和二氧化硫性質,明確二氧化硫的漂白性與次氯酸的漂白性根本區別.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)→2H2O(l)+Q1 2H2(g)+O2(g)→2H2O(g)+Q2 | |
| B. | S(g)+O2(g)→SO2(g)+Q1 S(s)+O2(g)→SO2(g)+Q2 | |
| C. | C(s)+0.5O2(g)→CO(g)+Q1 C(s)+O2(g)→CO2(g)+Q2 | |
| D. | H2(g)+Cl2(g)→2HCl(g)+Q1 $\frac{1}{2}{H_2}$(g)+$\frac{1}{2}C{l_2}$(g)→HCl(g)+Q2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含有大量Al3+的溶液:Na+、NH4+、SO42-、Cl- | |
| B. | 含有大量OH-的溶液:Na+、Ca2+、SO42-、CO32- | |
| C. | 含有大量Fe3+的溶液:Na+、Mg2+、NO3-、SCN- | |
| D. | 含有大量NO3-的溶液:H+、Fe2+、SO42-、Cl- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含20.0g NaOH的稀溶液與稀鹽酸完全中和,放出28.7kJ的熱量,則稀醋酸和稀NaOH溶液反應的熱化學方程式為:NaOH(aq)+CH3COOH(aq)=CH3COONa(aq)+H2O(l);△H=-57.4kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金剛石,s);△H>0,則金剛石比石墨穩定 | |
| C. | 已知反應2H2(g)+O2(g)=2H2O(l);△H=-571.6kJ•mol-1,則H2的燃燒熱為571.6kJ•mol-1 | |
| D. | 已知2C(s)+2O2(g)=2CO2(g)△H1;2C(s)+O2(g)=2CO(g)△H2,則△H1<△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 配制過程只需要三種儀器即可完成 | |
| B. | 容量瓶用蒸餾水洗凈后必須烘干才能用于溶液的配制 | |
| C. | 所配得的NaClO消毒液物質的量濃度為3.99mol/L | |
| D. | 需要稱量的NaClO固體的質量為140g |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1Ll.00mol•L-1NaCl溶濃中NaCl分子數為NA | |
| B. | 標準狀況下,2.24L由N2和O2組成的混合氣體中所含的原子數為0.1NA | |
| C. | 常溫下,0.1molCl2溶于水時,轉移的電子效是0.1NA | |
| D. | 0.lmolFe與過量稀HNO3反應時,轉移的電子教為0.3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
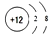
| A. | 35Cl-和37Cl-離子結構示意圖均可以表示為: | |
| B. | HClO的結構式:H-Cl-O | |
| C. | HF的電子式: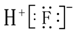 | |
| D. | 質子數為92、中子數為146的U原子:14692U |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 .
. .
.查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com