
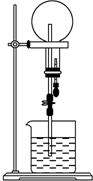
 已知NH3和HCl都是能用來做噴泉實驗的氣體.若在同溫同壓下用等體積燒瓶一個收集滿NH3,另一個收集HCl和N2的混合氣體,如圖所示.噴泉實驗停止后,兩個燒瓶內溶液的關系是(不考慮燒瓶內溶質的擴散,氨水的溶質按NH3計算)( )
已知NH3和HCl都是能用來做噴泉實驗的氣體.若在同溫同壓下用等體積燒瓶一個收集滿NH3,另一個收集HCl和N2的混合氣體,如圖所示.噴泉實驗停止后,兩個燒瓶內溶液的關系是(不考慮燒瓶內溶質的擴散,氨水的溶質按NH3計算)( )| A. | 溶質的物質的量濃度相同、溶質的質量分數不同 | |
| B. | 溶質的質量分數相同、溶質的物質的量濃度不同 | |
| C. | 溶質的物質的量濃度和溶質的質量分數都不同 | |
| D. | 溶質的物質的量濃度和溶質的質量分數都相同 |
分析 相同條件下氣體摩爾體積相同,設該條件下氣體摩爾體積為Vm,燒瓶的容積為VL,HCl和N2的混合氣體中氯化氫的體積為xL,則氯化氫和氨氣的物質的量為:n(NH3)=$\frac{V}{{V}_{m}}$mol,n(HCl)=$\frac{x}{{V}_{m}}$mol,氨氣極易溶于水,則反應后燒瓶中充滿溶液;收集HCl和N2的混合氣體燒瓶中,反應后溶液體積為xL,根據c=$\frac{n}{V}$可計算出兩溶液的濃度;由于溶質不同,溶液密度不同,根據c=$\frac{1000ρω}{M}$可知兩溶液中溶質質量分數不同.
解答 解:試題分析:設該條件下氣體摩爾體積為Vm,氣體的體積為V,因氣體極易溶于水,故溶液體積等于氣體的 體積.c=$\frac{n}{V}$=$\frac{\frac{V}{{V}_{m}}}{V}$=$\frac{1}{{V}_{m}}$,則不論NH3和HCl(N2不溶于水)是否充滿,物質的量濃度都等于$\frac{1}{{V}_{m}}$,因溶液中溶質質量和溶液質量不同,故溶質質量分數不同,
故選A.
點評 本題考查了氣體溶于水的物質的量濃度和質量分數的相關知識,題目難度中等,明確發生反應原理為解答關鍵,注意熟練掌握物質的量與物質的量濃度、氣體摩爾體積之間的關系.


科目:高中化學 來源: 題型:選擇題
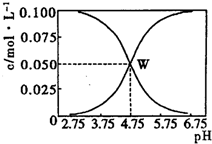 25℃時,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一組醋酸、醋酸鈉混合溶液,溶液中c(CH3COOH)、c(CH3COO-)與pH的關系如圖所示.下列有關溶液中離子濃度關系的敘述不正確的是( )
25℃時,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一組醋酸、醋酸鈉混合溶液,溶液中c(CH3COOH)、c(CH3COO-)與pH的關系如圖所示.下列有關溶液中離子濃度關系的敘述不正確的是( )| A. | 由題給圖示可求出25℃時醋酸的電離平衡常數Ka=10-4.75 | |
| B. | W點所表示的溶液中:c(Na+)+c(H+)=c(CH3COOH)+c(OH-) | |
| C. | pH=3.5的溶液中:c(Na+)+c(H+)-c(OH-)+c(CH3COOH)=0.1 mol•L-1 | |
| D. | 向W點所表示的1.0 L溶液中通入0.05 mol HCl氣體(溶液體積變化可忽略):c(H+)=c(CH3COOH))+c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | ③⑤ | D. | ③⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用溴水代替碘水進行萃取實驗 | |
| B. | 用過量的氯氣進行性質實驗 | |
| C. | 用乙烯和氧氣在銀作催化劑的條件下制備環氧乙烷 | |
| D. | 用銅粉代替銅絲進行銅和濃硝酸反應的實驗 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 少量金屬鈉保存在煤油里 | |
| B. | 液溴應保存在棕色磨口玻璃塞的試劑瓶中,并加少量水進行水封 | |
| C. | 為防止氧化,FeSO4溶液存放在加有少量銅粉的試劑瓶中 | |
| D. | 硝酸應裝在棕色瓶中密封避光保存 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 氯化鋅溶液中投入鈉 | B. | 氯化鐵溶液中投入銅 | ||
| C. | 硝酸銀溶液中投入銅 | D. | 硫酸銅溶液中投入鐵 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2種 | B. | 5種 | C. | 6種 | D. | 9種 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A | B | C | |
| 起始時合金粉末的質量/mg | 204 | 399 | 561 |
| 反應結束時生成氣體的體積/mL | 224 | 336 | 336 |
| A. | 起始時鹽酸的濃度為1mol•L-1 | B. | 加入的NaOH溶液為40mL | ||
| C. | 合金中鎂、鋁的物質的量相等 | D. | 所得的濾液中含三種陰離子 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com