
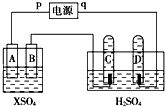
 如圖,p、q為直流電源的兩極,A由+2價金屬單質X制成,B、C、D為鉑電極,接通電源,金屬X沉積于B極,同時C、D極上均產生氣泡,試回答:
如圖,p、q為直流電源的兩極,A由+2價金屬單質X制成,B、C、D為鉑電極,接通電源,金屬X沉積于B極,同時C、D極上均產生氣泡,試回答:分析 (1)接通電源,金屬M沉積于B極,同時C、D產生氣泡,則B為陰極,M離子在陰極放電生成金屬單質,則A、C是陽極,B、D是陰極,連接陽極的是電源正極;
(2)C電極是電解池陽極,陽極上氫氧根離子放電;
(3)B上金屬離子得電子生成單質,A電極上X失電子生成金屬陽離子;
(4)根據金屬和轉移電子之間的關系式計算.
解答 解:(1)接通電源,金屬M沉積于B極,同時C、D產生氣泡,則B為陰極,M離子在陰極放電生成金屬單質,則A、C是陽極,C陽極上氫氧根離子失電子生成氧氣,B、D是陰極,所以p是正極,A電極上失電子發生氧化反應,
故答案為:正;氧氣;
(2)C是陽極,陽極上氫氧根離子放電生成氧氣,電極反應式為:4OH--4e-=O2↑+2H2O,故答案為:4OH--4e-=O2↑+2H2O;
(3)B上金屬離子得電子生成單質,A電極上X失電子生成金屬陽離子,溶液中離子濃度不變,所以溶液的pH不變,故答案為:不變;
(4)設其摩爾質量為M,
電解時,B電極上的電極反應式為:X 2++2e-=X
2mol 1mol
0.004mol $\frac{0.128g}{M}$
M=$\frac{0.128g×2mol}{0.004mol×1mol}$=64g/mol,
故答案為:64g/mol.
點評 本題涉及原電池、電解池的工作原理以及電極反應式的書寫和電子守恒的應用知識,屬于綜合知識的考查,難度中等,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 碳酸鈉與鹽酸反應 | B. | 氧化鐵與一氧化碳在高溫下反應 | ||
| C. | 氧化銅與硫酸反應 | D. | 鐵粉與硫酸銅溶液反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 A、B、X、Y、Z是前四周期的常見元素,原子序數依次增大,A可形成自然界硬度最大的單質;B與A同周期,核外有三個未成對電子;X原子的第一電離能至第四電離能分別是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常溫常壓下,Y單質是固體,其氧化物是形成酸雨的主要物質;Z的一種同位素的質量數為63,中子數為34,請回答:
A、B、X、Y、Z是前四周期的常見元素,原子序數依次增大,A可形成自然界硬度最大的單質;B與A同周期,核外有三個未成對電子;X原子的第一電離能至第四電離能分別是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常溫常壓下,Y單質是固體,其氧化物是形成酸雨的主要物質;Z的一種同位素的質量數為63,中子數為34,請回答:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c(H2S) | |
| B. | Na2C2O4溶液:c(OH-)═c(H+)+c(HC2O4-)+2c(H2C2O4) | |
| C. | Na2CO3溶液:c(Na+)+c(H+)═2c(CO32-)+c(OH-) | |
| D. | CH3COONa和CaCl2溶液:c(Na+)+c(Ca2+)═c(CH3COO-)+c(OH-)+c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1個 | B. | 2個 | C. | 3個 | D. | 4個 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
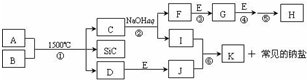 如圖是一些常見元素的單質或化合物之間的轉化關系.溶液中的水以及部分反應物或生成物未標出.A、E是空氣中的兩種主要成分,C是由兩種元素組成的新型材料,并且C的原子數、最外層電子數之和與SiC相同,J是一種能引起溫室效應的氣體,K是兩性化合物.反應③、④、⑤用于工業中生產H.
如圖是一些常見元素的單質或化合物之間的轉化關系.溶液中的水以及部分反應物或生成物未標出.A、E是空氣中的兩種主要成分,C是由兩種元素組成的新型材料,并且C的原子數、最外層電子數之和與SiC相同,J是一種能引起溫室效應的氣體,K是兩性化合物.反應③、④、⑤用于工業中生產H.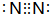 ,G的化學式NO;
,G的化學式NO;查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com