
 根據氧化還原反應Zn+2H+═Zn2++H2↑設計的原電池如圖所示:
根據氧化還原反應Zn+2H+═Zn2++H2↑設計的原電池如圖所示:分析 根據氧化還原反應Zn+2H+═Zn2++H2↑設計的原電池,Zn失電子作負極,Cu為正極,正極上氫離子得電子,電子從負極流向正極,電流從正極流向負極,結合電子與物質的關系計算.
解答 解:(1)根據氧化還原反應Zn+2H+═Zn2++H2↑設計的原電池,Zn失電子作負極,負極反應為Zn-2e-=Zn2+;Cu為正極,正極上氫離子得電子生成氫氣,則正極反應為2H++2e-=H2↑;
故答案為:負;Zn-2e-=Zn2+;正;2H++2e-=H2↑;
(2)外電路中,電子的流向從Zn電極向Cu電極;電流的流動方向由Cu電極流向 Zn電極;
故答案為:Zn;Cu;Cu;Zn;
(3),負極反應為Zn-2e-=Zn2+,正極反應為2H++2e-=H2↑,當電路中轉移0.2mol的電子時,消耗的Zn為0.1mol,則鋅的質量為6.5g,生成的氫氣為0.1mol,其體積為2.24L;
故答案為:6.5g;2.24L.
點評 本題考查原電池的設計及工作原理,注意電極反應式的書寫方法,牢固掌握原電池中電極的判斷,電極反應式的書寫的方法性問題,側重于考查學生的分析能力和計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | HCl的電子式為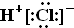 | B. | Cl-的結構示意圖 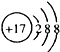 | ||
| C. | CO2的電子式 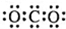 | D. | 質量數為37的氯原子 ${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | NH4Cl?NH4++Cl- | B. | H2S?2H++S2- | ||
| C. | KHCO3?K++H+++CO3- | D. | CH3COONH4=NH4++CH3COO- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 甲醛 | B. | 乙醛 | C. | 丁醛 | D. | 戊醛 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某校開展課外研究性學習:從廢舊干電池中回收碳棒、MnO2、NH4Cl、ZnCl2等物質,整個過程如下,回答有關問題:
某校開展課外研究性學習:從廢舊干電池中回收碳棒、MnO2、NH4Cl、ZnCl2等物質,整個過程如下,回答有關問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com