
分析 (1)利用n=$\frac{N}{{N}_{A}}$來計算氯離子的物質的量,再由化學式可確定MCl2的物質的量,然后利用M=$\frac{m}{n}$計算摩爾質量,最后計算M的相對原子質量;
(2)CO(NH2)2與H2O分子中都含有1個O原子,二者含有氧原子數目相等,則二者物質的量相等;
(3)先根據n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$計算各物質的物質的量,然后根據物質的組成求出氫原子個數.
解答 解:(1)氯離子的物質的量為$\frac{3.01×1{0}^{23}}{6.02×1{0}^{23}}$=0.5mol,MCl2的物質的量為0.5mol×$\frac{1}{2}$=0.25mol,則MCl2的摩爾質量為$\frac{23.75g}{0.25mol}$=95g/mol,
MCl2的相對分子質量為95,設M的相對原子質量為x,則x+35.5×2=95,解得x=24,
故答案為:95g/mol;95;24;
(2)CO(NH2)2與H2O分子中都含有1個O原子,二者含有氧原子數目相等,則二者物質的量相等,即2mol CO(NH2)2中含氧原子與2mol水含有氧原子數目相等,所以水的質量為:m(H2O)=n×M=2mol×18g/mol=36g,
故答案為:36;
(3)①標準狀況下22.4L CH4的物質的量$\frac{22.4L}{22.4L/mol}$=1mol,所含的氫原子數為4mol;
②1.5mol NH3所含的氫原子數為4.5mol;
③1.806×1024個H2O的物質的量=$\frac{N}{{N}_{A}}$=$\frac{1.806×1{0}^{24}}{6.02×1{0}^{23}}$=3mol,所含的氫原子數為6mol;
④標準狀況下,73g HCl的物質的量=$\frac{73g}{36.5g/mol}$=2mol,所含的氫原子數為2mol,所含H原子個數由多到少的順序是:③>②>①>④,
故答案為:③>②>①>④;
點評 本題考查有關物質的量的計算,明確n=$\frac{m}{M}$=$\frac{V}{{V}_{m}}$=$\frac{N}{{N}_{A}}$等計算公式的理解與靈活應用是解答本題的關鍵,并注意摩爾質量與相對分子質量的關系,注意對化學式意義的理解,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 硒元素的非金屬性比溴元素的弱 | |
| B. | 硒的最高價氧化物的水化物的分子式為:H2SeO3 | |
| C. | 硒在周期表中位于第五周期VIA族 | |
| D. | 硒的氣態氫化物的穩定性比硫化氫強 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X的離子半徑>Y的離子半徑 | |
| B. | Z的氫化物穩定性>W的氫化物穩定性 | |
| C. | 化合物X2W2和Y2W3中都不含配位鍵 | |
| D. | 1 mol ZW2晶體所含Z-W鍵的數目為4NA |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
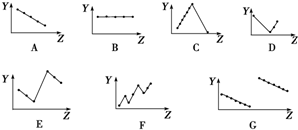
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 分子式為C10H14的一元取代芳烴,其可能的結構有5種 | |
| B. | 分子式為C2H4O的只能表示一種物質 | |
| C. | 甲酸甲酯能發生銀鏡反應,并與丙酸互為同系物 | |
| D. | 丙烯在一定條件下與水反應主要產物是2-丙醇 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬性:Na<Mg<Al | B. | 熱穩定性:HCl>H2S>PH3 | ||
| C. | 酸性強弱:H2CO3<HSO4<HClO4 | D. | 熔點:Na>K>Rb |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 淀粉、油脂、蛋白質都能水解,但水解產物不同 | |
| B. | 大豆富含蛋白質,故豆漿煮沸后蛋白質變成了氨基酸 | |
| C. | 石油的分餾、煤的氣化、海水提溴的過程都包含化學變化 | |
| D. | 地淘油經處理后可作為汽車燃油,故地溝油的成分是液態烴 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com