
 二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑.回答下列問題:
二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑.回答下列問題:分析 (1)KClO3在H2SO4存在下與Na2SO3反應,SO32-被氧化成SO42-,由電子、電荷守恒可知該離子反應為2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O;
(2)由信息可知,ClO2易溶于水,所以不能利用水溶液吸收,氨氣為堿性氣體,利用性質差異分離提純;
(3)①由題目信息可知,ClO2通入錐形瓶與酸性碘化鉀溶液反應,氧化I-為I2,自身被還原為Cl-,同時生成水;
②玻璃液封裝置可防止有害氣體逸出;
③根據關系式2ClO2~5I2~10Na2S2O3計算n(ClO2),再根據m=nM計算m(ClO2);
(4)亞氯酸鹽具有氧化性,Fe2+將ClO2-還原成Cl-,Fe2+ 被氧化為鐵離子.
解答 解:(1)KClO3在H2SO4存在下與Na2SO3反應制得ClO2,可知SO32-被氧化成SO42-,由電子、電荷守恒可知該離子反應為2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O,氧化劑為KClO3還原產物為ClO2 ,還原劑為Na2SO3,被氧化得到氧化產物SO42-,由離子反應可知該反應氧化產物與還原錯誤物質的量之比為1:2,
故答案為:1:2;
(2)A.ClO2易溶于水,不能利用水吸收氨,故A錯誤;
B.濃硫酸可以吸收氨氣,且不影響ClO2,故B正確;
C.堿石灰不能吸收氨氣,故C錯誤;
D.ClO2易溶于水,不能利用飽和食鹽水吸收氨氣,故D錯誤;
故答案為:B;
(3)①由題目信息可知,ClO2通入錐形瓶與酸性碘化鉀溶液反應,氧化I-為I2,自身被還原為Cl-,同時生成水,反應離子方程式為2ClO2+10I-+8H+═2Cl-+5I2+4H2O,
故答案為:2ClO2+10I-+8H+═2Cl-+5I2+4H2O;
②玻璃液封裝置的作用是吸收殘留的ClO2氣體避免碘的逸出,
故答案為:吸收殘留的ClO2氣體;
③含有Na2S2O3物質的量為0.02 L×0.1mol/L=0.002 mol,則:
根據關系式:2ClO2~5I2~10Na2S2O3,
2 10
n(ClO2) 0.002mol
所以n(ClO2)=0.0004mol,
所以m(ClO2)=0.004 mol×67.5g/mol=0.02700g,
故答案為:0.02700;
(4)若要除去超標的亞氯酸鹽,AD均不能還原亞氯酸鹽,B中KI具有還原性但氧化產物不適合飲用水使用,只有C中Fe2+將ClO2-還原成Cl-,Fe2+ 被氧化為鐵離子,且鐵離子水解生成膠體可凈化飲用水,則最適宜的是C,
故答案為:C.
點評 本題考查物質含量的測定,為高頻考點,把握物質的性質、制備流程、發生的反應為解答的關鍵,側重分析與實驗、計算能力的綜合考查,綜合性較強,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
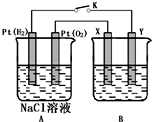 某化學興趣小組用下圖所示裝置進行電化學原理的實驗探究,回答下列問題:
某化學興趣小組用下圖所示裝置進行電化學原理的實驗探究,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
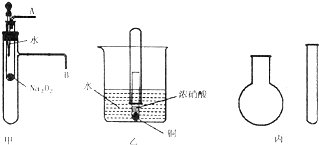 “套管實驗”是將一支較小的玻璃儀器裝入另一支玻璃儀器中,經組裝來完成原來需要較多儀器進行的實驗.因其具有許多優點,已被廣泛應用于化學實驗中.下列三個實驗均為“套管實驗”,請觀察、分析,回答下列問題:
“套管實驗”是將一支較小的玻璃儀器裝入另一支玻璃儀器中,經組裝來完成原來需要較多儀器進行的實驗.因其具有許多優點,已被廣泛應用于化學實驗中.下列三個實驗均為“套管實驗”,請觀察、分析,回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向0.10mol/L NH4HCO3中溶液中通入CO2:c(NH4+)=c(HCO3-)+c(CO32-) | |
| B. | 向0.10mol/L NaHSO3中溶液中通入NH3:c(Na+)>c(NH4+)>c(SO32-) | |
| C. | 向0.10mol/L Na2SO3中溶液中通入SO2:c(Na+)=2[c(H2SO3)+c(HSO3-)+c(SO32-)] | |
| D. | 向0.10mol/L CH3COONa中溶液中通入HCl:c(Na+)>c(CH3COOH)=c(Cl-) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CO2氣體通入Na2SiO3溶液中 | B. | CO2氣體通入飽和Na2CO3溶液中 | ||
| C. | SO2氣體通入BaCl2溶液中 | D. | SO2氣體通入Ba(OH)2溶液中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Ba(OH)2═Ba2++2OH- | B. | AlCl3═Al3++Cl3- | ||
| C. | H2SO4═2H++S6++4O2- | D. | Na2CO3═Na2++CO32- |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 用氫氧化鈉溶液除去鎂粉中的鋁粉:2Al+2OH-═AlO2-+H2↑ | |
| B. | 向碳酸氫鈉溶液中加入少量氫氧化鈣:2HCO3-+Ca2++2OH-═CaCO3↓+CO32-+2H2O | |
| C. | 氧化鐵溶于氫碘酸:Fe2O3+6H+═2Fe3++3H2O | |
| D. | Na2S溶液顯堿性:S2-+H2O?HS-+OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 中子數為20的氯原子:${\;}_{17}^{20}$Cl | B. | NH3分子的電子式: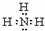 | ||
| C. | 鋁原子的結構示意圖: | D. | 聚丙烯的結構簡式為: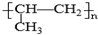 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com