
| A. | 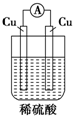 | B. | 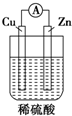 | C. | 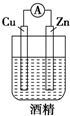 | D. | 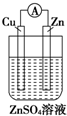 |
科目:高中化學 來源: 題型:選擇題
| A. | 改變條件,反應物的轉化率增大,平衡常數也一定增大 | |
| B. | 常溫下,V1L pH=12的NaOH溶液與V2L pH=2的HA溶液混合,若混合液顯中性,則V1≤V2 | |
| C. | 在0.1mol•L-1 NaHCO3溶液中,加入少量NaOH固體,Na+和CO32-的離子濃度均增大 | |
| D. | 反應2NO2(g)?N2O4(g)△H<O,升高溫度該反應平衡常數增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 括號內為雜項 | 除雜試劑 | 除雜操作 | |
| A | Na2O2(Na2O) | O2 | 在純氧中加熱 |
| B | Na2CO3(NaHCO3) | CO2 | 通入過量的CO2 |
| C | FeCl(FeCl2) | Cl2 | 通入過量的Cl2 |
| D | FeSO4(CuSO4) | Fe | 加入過量的Fe粉,充分反應后過濾 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常數K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
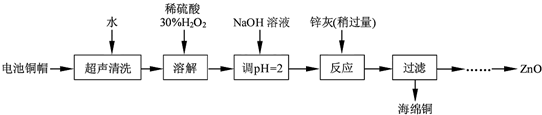
| 開始沉淀的pH | 完全沉淀的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
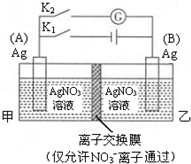
| A. | 閉合K1,斷開K2后,A電極增重 | |
| B. | 閉合K1,斷開K2后,乙池溶液中Ag+濃度增大 | |
| C. | 斷開K1,閉合K2后,B電極發生氧化反應 | |
| D. | 斷開K1,閉合K2后,NO3-向A電極移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 乙烯使溴水褪色 | B. | 乙醇與濃硫酸共熱至170℃ | ||
| C. | 溴乙烷與NaOH水溶液共熱 | D. | 在液溴與苯的混合物中撒入鐵粉 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
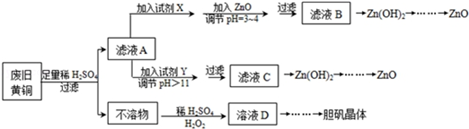
| Fe3+ | Fe2+ | Zn2+ | |
| 開始沉淀的pH | 1.1 | 5.8 | 5.9 |
| s沉淀完全的pH | 3.0 | 8.8 | 8.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鐵與鹽酸反應:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 大理石和醋酸:CO32-+2H+═H2O+CO2↑ | |
| C. | 銅片插入硝酸銀溶液中:Cu+Ag+═Cu2++Ag | |
| D. | 向Ba(OH)2溶液中滴加KHSO4溶液至中性:Ba2++2OH-+2H++SO42-═BaSO4↓+2H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com