
| A. | 0.01mol•L-1 | B. | 0.05mol•L-1 | C. | 0.017mol•L-1 | D. | 0.50mol•L-1 |
分析 物質的量濃度相等的NaOH和HCl溶液,以3:2體積比相混合,發生反應:NaOH+HCl=NaCl+H2O,氫氧化鈉有剩余,令二者的濃度為cmol/L,用c表示出反應后溶液中c(OH-),根據混合后溶液的pH=13,可知應后溶液中c(OH-)=0.1mol/L,據此計算.
解答 解:物質的量濃度相等的NaOH和HCl溶液,以3:2體積比相混合,發生反應:NaOH+HCl=NaCl+H2O,氫氧化鈉有剩余,令二者的濃度為cmol/L,則反應后溶液中c(OH-)=$\frac{3c-2c}{3+2}$mol/L=$\frac{c}{5}$mol/L,根據混合后溶液的pH=13,可知應后溶液中c(OH-)=0.1mol/L,即$\frac{c}{5}$mol/L=0.1mol/L,解得c=0.5,
故選D.
點評 本題考查溶液pH值的有關計算,難度不大,注意酸堿混合后呈堿性,先計算剩余氫氧根的濃度,再計算氫離子濃度,利用定義計算pH值.


 七星圖書口算速算天天練系列答案
七星圖書口算速算天天練系列答案 初中學業考試導與練系列答案
初中學業考試導與練系列答案科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 該反應的化學平衡常數表達式為:K=$\frac{c(CO)•({H}_{2}O)}{c(C{O}_{2})•({H}_{2})}$ | |
| B. | 升高溫度,正反應速率增大,逆反應速率減小 | |
| C. | 容器內CO和H20的濃度始終相等 | |
| D. | 容器內的壓強始終不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①② | B. | ①④ | C. | ①③ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
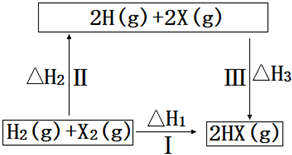
| A. | 2H(g)+2X(g)=2HX(g)△H3<0 | |
| B. | 途徑Ⅰ生成HX的反應熱與途徑無關,所以△H1=△H2+△H3 | |
| C. | 途徑Ⅰ生成HBr放出的熱量比生成HCl的少,說明HBr比HCl穩定 | |
| D. | Cl、Br、I的非金屬性依次減弱,所以途徑Ⅱ吸收的熱量依次減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 常溫下,0.1 mol•L-1 HA溶液的pH=3,則HA的電離:HA=H++A- | |
| B. | 用銅電極電解飽和硫酸銅溶液:2Cu2++2H2O$\frac{\underline{\;通電\;}}{\;}$2Cu+O2↑+4H+ | |
| C. | 向1 mL 2 mol•L-1NaOH溶液中滴加1~2滴0.1 mol•L-1MgCl2溶液后,再滴加2滴0.1 mol•L-1 FeCl3溶液:Mg2++2OH-═Mg(OH)2↓,3Mg(OH)2+2Fe3+═2Fe(OH)3+3Mg2+ | |
| D. | 鋼鐵發生吸氧腐蝕生成鐵銹:2Fe+O2+2H2O═2Fe(OH)2,4Fe(OH)2+O2+2H2O═4Fe(OH)3,2Fe(OH)3═Fe2O3•xH2O+(3-x)H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=6的NaHSO4溶液:c(Na+)+c(H+)=2c(SO42-)+c(OH-) | |
| B. | 0.1 mol/L NaHCO3溶液加水稀釋后,c(H+)與c(OH-)的乘積不變 | |
| C. | pH相同的①CH3COONa、②NaClO二種溶液的c(Na+):①<② | |
| D. | 0.1 mol/L Na2SO3溶液:c(Na+)=2c(SO32-)+2c(HSO3-)+2c(H2SO3) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 | Cu(OH)2 | Zn(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 10.4 | 6.7 | 8.0 |
| 沉淀物 | CuS | ZnS | MnS | FeS | ||
| Ksp | 8.5×10-45 | 1.2×10-23 | 1.4×10-15 | 3.7×10-14 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com