
| A. | Zn2+、Cu、Fe3+ | B. | Zn、Cu2+、Fe3+ | ||
| C. | Zn2+、Cu2+、Cu、Fe2+ | D. | Zn2+、Cu2+、Fe、Fe2+ |
分析 相同物質的量的硫酸銅、氯化鐵和Zn置于水中充分反應后,由氧化性:Fe3+>Cu2+>Fe2+,所以Zn先與Fe3+反應,為Zn+2Fe3+=Zn2++2Fe2+,剩余的Zn再與Cu2+反應,以此來解答.
解答 解:因氧化性:Fe3+>Cu2+>Fe2+,所以Zn先與Fe3+反應,為Zn+2Fe3+=Zn2++2Fe2+,
設硫酸銅、氯化鐵和鋅的物質的量為1mol,Zn+2Fe3+=Zn2++2Fe2+反應完后剩余的Zn為0.5mol,
再與Cu2+反應,發生Zn+Cu2+=Zn2++Cu,則Cu2+有剩余,
所以溶液中存在Zn2+、Cu2+、Fe2+還有Cu生成,
故選C.
點評 本題考查物質的性質及氧化還原反應,為高頻考點,把握氧化性的強弱及反應先后順序為解答的關鍵,側重分析與應用能力的考查,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | 1:10:100:1 000 | B. | 0:1:12:11 | C. | 14:13:12:11 | D. | 14:13:2:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 平衡常數不隨反應物或生成物的濃度的改變而改變 | |
| B. | 平衡常數隨溫度的改變而改變 | |
| C. | K值越大,反應進行的程度越大 | |
| D. | 溫度越高,K值越大 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中發生反應:N2O4(g)?2NO2(g)△H>0,反應過程中各物質的物質的量濃度(c)隨時間(t)的變化曲線如圖所示.
在恒溫恒容條件下,將一定量NO2和N2O4的混合氣體通入容積為2L的密閉容器中發生反應:N2O4(g)?2NO2(g)△H>0,反應過程中各物質的物質的量濃度(c)隨時間(t)的變化曲線如圖所示.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③ | B. | ②④ | C. | ③④⑤ | D. | ①③⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
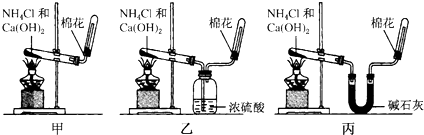
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com