
| 1 |
| 3 |


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:
| c(H+) |
| c(OH-) |
| A、在25℃時,若溶液呈中性,則pH=7,AG=1 |
| B、在25℃時,若溶液呈酸性,則pH<7,AG<0 |
| C、在25℃時,若溶液呈堿性,則pH>7,AG>0 |
| D、在25℃時,溶液的pH與AG的換算公式為AG=2(7-pH) |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、CuSO4?5H2O是一種化合物 |
| B、分散系一定是混合物 |
| C、堿性氧化物不一定是金屬氧化物 |
| D、氯化銀、冰醋酸、酒精、水銀分別屬于強電解質、弱電解質、非電解質、既不是電解質也不是非電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、常溫常壓下,3.0g甲醛(CH2O)和冰醋酸(C2H4O2)的混合物中含有的原子總數為0.4NA |
| B、在標準狀況下,22.4LCl2和HCl的混合氣體中含有的分子總數為2×6.02×1023 |
| C、500mL1mol/L的Na2SO4溶液中,Na+和SO42-離子總數為6.02×1023 |
| D、標準狀況下,1molCCL4的體積為22.4L |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
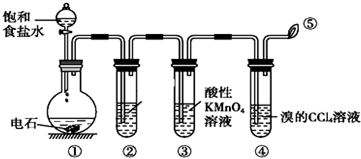
查看答案和解析>>
科目:高中化學 來源: 題型:
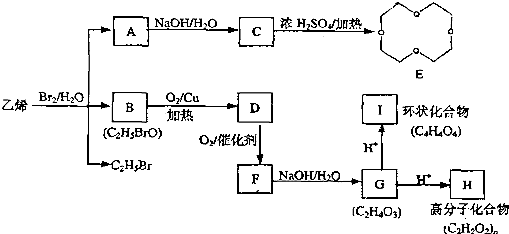
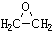 )的結構可簡寫為
)的結構可簡寫為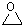 ,則E的分子式是
,則E的分子式是查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com