
分析 ①測得溶液A、C、E呈堿性,三種溶液為堿液或水解呈堿性的溶液,且堿性為A>E>C,則A為堿,溶液中含有大量的OH-離子,OH-離子與Ag+,Ca2+,Fe2+,Al3+等離子不能大量共存,故A只能為Ba(OH)2,根據越弱越水解,E應為碳酸鹽,根據離子共存,只能為K2CO3,C為醋酸鹽;
②向B溶液中滴加稀氨水,先出現沉淀,繼續滴加氨水,沉淀消失,則B中含有銀離子,應為硝酸銀溶液,加入氨水發生的反應為AgNO3+NH3•H2O=AgOH↓+NH4NO3、AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O;
③向D溶液中滴加Ba(NO3)2溶液,無明顯現象,說明D中不含SO42-離子;
④向F溶液中滴加氨水,生成白色絮狀沉淀,沉淀迅速變成灰綠色,最后變成紅褐色,說明F中含有Fe2+離子;
綜上分析可知,A為Ba(OH)2,B為AgNO3,C為Ca(CH3COO)2,D為AlCl3,E為K2CO3,F為FeSO4,以此來解答.
解答 解:①測得溶液A、C、E呈堿性,三種溶液為堿液或水解呈堿性的溶液,且堿性為A>E>C,則A為堿,溶液中含有大量的OH-離子,OH-離子與Ag+,Ca2+,Fe2+,Al3+等離子不能大量共存,故A只能為Ba(OH)2,根據越弱越水解,E應為碳酸鹽,根據離子共存,只能為K2CO3,C為醋酸鹽;
②向B溶液中滴加稀氨水,先出現沉淀,繼續滴加氨水,沉淀消失,則B中含有銀離子,應為硝酸銀溶液,加入氨水發生的反應為AgNO3+NH3•H2O=AgOH↓+NH4NO3、AgOH+2NH3•H2O=Ag(NH3)2OH+2H2O;
③向D溶液中滴加Ba(NO3)2溶液,無明顯現象,說明D中不含SO42-離子;
④向F溶液中滴加氨水,生成白色絮狀沉淀,沉淀迅速變成灰綠色,最后變成紅褐色,說明F中含有Fe2+離子;
綜上分析可知,A為Ba(OH)2,B為AgNO3,C為Ca(CH3COO)2,D為AlCl3,E為K2CO3,F為FeSO4.
(1)由上述分析可知,B為硝酸銀,故答案為:硝酸銀(或AgNO3);
(2)E應為碳酸鹽,六種陽離子中可以與碳酸根形成可溶性鹽的只有鉀離子,故E為K2CO3,
故答案為:碳酸鉀;由①中堿性強弱的順序可知,E是碳酸鹽,六種陽離子中可以與碳酸根形成可溶性鹽的只有鉀離子,所以E是碳酸鉀;
(3)根據以上分析可知A為Ba(OH)2,C為Ca(CH3COO)2,D為AlCl3,故答案為:Ba(OH)2;Ca(CH3COO)2;AlCl3.
點評 本題考查無機物的推斷,為高頻考點,把握離子之間的反應、鹽類水解、沉淀的判斷等為解答的關鍵,側重分析與推斷能力的考查,題目難度不大.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②④ | B. | ①③⑤ | C. | ②③⑤ | D. | 只有③ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 某校高三同學高考前重做以下兩個課本實驗,請你回答實驗過程中的相關問題:
某校高三同學高考前重做以下兩個課本實驗,請你回答實驗過程中的相關問題:| 編號 | 溫度/℃ | H2SO4體積/mL | KI溶液體積/mL | H2O體積/mL | 淀粉溶液 /mL | 出現藍色時間/s |
| A | 39 | 10 | 5 | 5 | 1 | 5 |
| B | TB | 10 | 5 | 5 | 1 | 沒出現藍色 |
| C | 5 | 10 | 5 | 5 | 1 | 39 |
| D | t |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
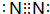
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
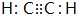 ;D的最簡式CH2=CH2;
;D的最簡式CH2=CH2; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反應類型為取代反應.B→C的化學方程式nCH2=CHCl$\stackrel{催化劑}{→}$
+HBr,其反應類型為取代反應.B→C的化學方程式nCH2=CHCl$\stackrel{催化劑}{→}$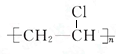 ,其反應類型為加聚反應.
,其反應類型為加聚反應.
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com