
| A. | 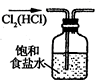 除去Cl2中HCl | B. | 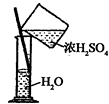 稀釋濃H2SO4 | C. | 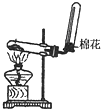 制取氧氣 | D. | 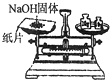 稱取NaOH |
科目:高中化學 來源: 題型:解答題
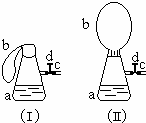 如圖(Ⅰ)中錐形瓶a內放入43.8g10%的稀鹽酸,b是未充氣的氣球,里邊放有4g碳酸鈣粉末,將它緊緊套在瓶a口上,膠管c套在瓶的側口,并用彈簧夾d夾緊(瓶口和側口都不漏氣).將圖Ⅰ的裝置在托盤天平上稱量,質量為W1克.根據實驗現象填寫下列空白:
如圖(Ⅰ)中錐形瓶a內放入43.8g10%的稀鹽酸,b是未充氣的氣球,里邊放有4g碳酸鈣粉末,將它緊緊套在瓶a口上,膠管c套在瓶的側口,并用彈簧夾d夾緊(瓶口和側口都不漏氣).將圖Ⅰ的裝置在托盤天平上稱量,質量為W1克.根據實驗現象填寫下列空白:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
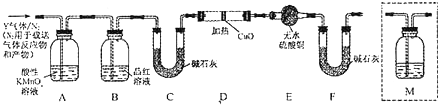
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
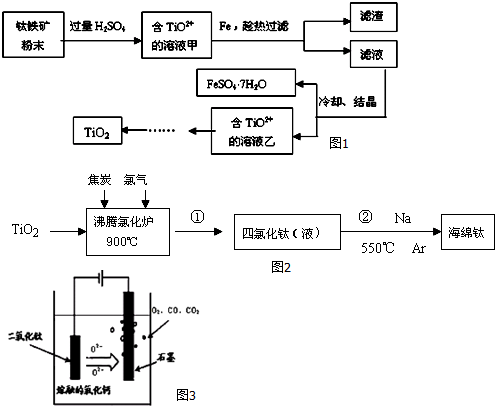
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
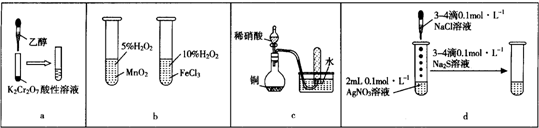
| A. | a圖示裝置,滴加乙醇試管中橙色溶液變為綠色,乙醇發生消去反應生成乙酸 | |
| B. | b圖示裝置,右邊試管中產生氣泡迅速,說明氯化鐵的催化效果比二氧化錳好 | |
| C. | c圖示裝置,根據試管中收集到無色氣體,驗證銅與稀硝酸的反應產物是NO | |
| D. | d圖示裝置,試管中先有白色沉淀、后有黑色沉淀,不能驗證AgCl的溶解度大于Ag2S |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 ,P元素屬于ds區元素.
,P元素屬于ds區元素.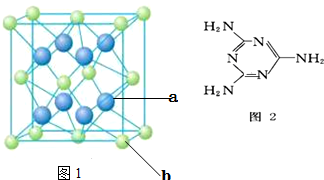
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
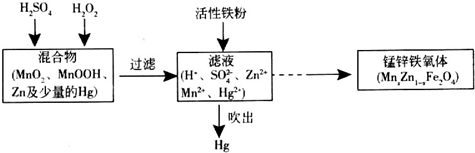
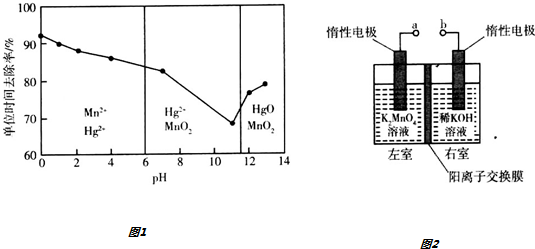
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com