
分析 (1)依據元素守恒計算氯化亞鐵和氯化鐵物質的量之比,進一步計算氯化鐵質量分數;金屬鐵和鹽酸反應生成氯化亞鐵和氫氣,金屬鐵和氯氣之間反應生成氯化鐵;
(2)用FeCl3與KClO在強堿性條件下反應制取K2FeO4;
(3)K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,正極上FeO42-得電子和H2O反應生成Fe(OH)3.
解答 (1)解:(1)FeCl2和FeCl3的混合物的樣品中FeCl2物質的量為x,FeCl3的物質的量為y,則(x+y):(2x+3y)=1:2.1,得到x:y=9:1,氯化鐵物質的量分數=$\frac{9}{1+9}$×100%=9%;金屬鐵和鹽酸反應生成氯化亞鐵和氫氣,金屬鐵和氯氣之間反應生成氯化鐵;
故答案為:90%;鹽酸;氯氣;
(2)用FeCl3與KClO在強堿性條件下反應制取K2FeO4,反應的離子方程式為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+5H2O+3Cl-或2Fe3++10OH-+3ClO-=2FeO42-+5H2O+3Cl-,故答案為:2Fe(OH)3+3ClO-+4OH-=2FeO42-+5H2O+3Cl-或2Fe3++10OH-+3ClO-=2FeO42-+5H2O+3Cl-;
(3)K2FeO4-Zn也可以組成堿性電池,K2FeO4在電池中作為正極材料,正極上FeO42-得電子和H2O反應生成Fe(OH)3,電極反應式為FeO42-+3e-+4H2O=Fe(OH)3+5 OH-;故答案為:FeO42-+3e-+4H2O=Fe(OH)3+5OH-.
點評 本題考查物質的性質、電極反應式的書寫,為高頻考點,明確各個電極上發生的反應是解本題關鍵,難點是電極反應式的書寫,注意結合電解質溶液酸堿性書寫,題目難度中等.


 開心快樂假期作業暑假作業西安出版社系列答案
開心快樂假期作業暑假作業西安出版社系列答案 名題訓練系列答案
名題訓練系列答案科目:高中化學 來源: 題型:選擇題
| A. | H2和O2反應生成水 | B. | 鋅片投入稀硫酸中 | ||
| C. | 木炭在高溫下與CO2反應生成CO | D. | 2KClO3$\frac{\underline{\;MnO_{2}\;}}{△}$2KCl+3O2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.1 mol•L-1 CH3COOH溶液與0.1 mol•L-1NaOH溶液等體積混合 | |
| B. | 向40mL0.2 mol•L-1的NaOH溶液中通入67.2mLCO2(標況) | |
| C. | 在100mL1 mol•L-1NH4Cl溶液中,投入3.9gNa2O2 | |
| D. | 在20mL0.01 mol•L-1Ma(HCO3)2溶液中,投入0.2g Ma(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
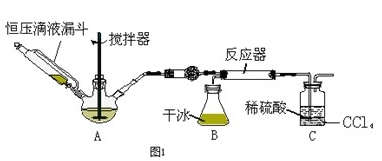
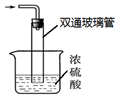
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、SO42-、NH4+、CO32- | B. | K+、Ba2+、OH-、Cl- | ||
| C. | Na+、H+、Cl-、SO42- | D. | Na+、Mg2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | K+、Ag+、NO3-、Cl- | B. | NH4+、Ba2+、Cl-、CO32- | ||
| C. | H+、Ca2+、CO32-、NO3- | D. | Na+、Al3+、SO42-、NO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 蒸發溶劑 | B. | 升高溫度 | C. | 降低溫度 | D. | 加入KN03固體 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
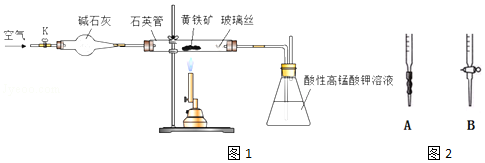
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com