
 高純MnCO3是制備高性能磁性材料的主要原料.實驗室以MnO2為原料制備少量高純MnCO3的操作步驟如下:
高純MnCO3是制備高性能磁性材料的主要原料.實驗室以MnO2為原料制備少量高純MnCO3的操作步驟如下:分析 (1)①根據實驗裝置圖可知,左邊集氣瓶的作用是混合SO2和N2;
②石灰乳的作用是吸收尾氣二氧化硫,堿和酸性氧化物反應得到對應的鹽和水;
③MnO2做氧化劑把亞硫酸氧化為硫酸,自身被還原為Mn2+,據此書寫反應的離子方程式;
④為使SO2盡可能轉化完全,一定要保證控制反應的溫度,在通入SO2和N2比例一定、不改變固液投料的條件下,要求所通氣體一定要慢;
(2)制取的原理是碳酸根和錳離子之間反應生成碳酸錳的過程,但要考慮MnCO3難溶于水、乙醇并在潮濕時易被空氣氧化,100℃開始分解以及Mn(OH)2開始沉淀時pH=7.7等因素,過程中控制溶液的PH值以及洗滌沉淀所選的溶劑要小心,據此答題.
解答 解:(1)①左邊集氣瓶的作用是混合SO2和N2 ,
故答案為:混合SO2和N2;
②石灰乳的作用是吸收尾氣二氧化硫,堿和酸性氧化物反應得到對應的鹽和水,反應為SO2+Ca(OH)2=CaSO3+H2O,
故答案為:SO2+Ca(OH)2=CaSO3+H2O;
③MnO2做氧化劑把亞硫酸氧化為硫酸,自身被還原為Mn2+,故反應的離子方程式為:MnO2+H2SO3=Mn2++SO42-+H2O,
故答案為:MnO2+H2SO3=Mn2++SO42-+H2O;
④使SO2盡可能轉化完全,應定要保證控制反應的溫度,在通入SO2和N2比例一定、不改變固液投料的條件下,要求所通氣體一定要慢,故選ac;
(2)制取的原理是碳酸根和錳離子之間反應生成碳酸錳的過程,但要考慮MnCO3難溶于水、乙醇并在潮濕時易被空氣氧化,100℃開始分解以及Mn(OH)2開始沉淀時pH=7.7等因素,過程中控制溶液的PH值以及洗滌沉淀所選的溶劑要小心,所以實驗步驟為邊攪拌邊加入碳酸鈉或碳酸氫鈉,并控制溶液的PH<7.7、過濾,用水洗滌2-3次、檢驗SO42-是否被除去,此時必須用鹽酸將溶液酸化,用少量的乙醇洗滌,
故答案為:過濾,水洗2~3次;是; C2H5OH.
點評 本題主要考查了制備高純碳酸錳實驗方案,讀懂工藝流程,正確識圖、理解離子反應的本質是解答的關鍵,本題實驗綜合性強,難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源:2017屆江蘇省高三上學期月考一化學試卷(解析版) 題型:選擇題
一種三室微生物燃料電池污水凈化系統原理如右圖所示,圖中有機廢水中有機物可用C6H10O5表示。下列有關說法正確的是

A.b電極為該電池的負極
B.b電極附近溶液的pH減小
C.a電極反應式:C6H10O5-24e-+7H2O===6CO2↑+24H+
D.中間室:Na+移向左室,Cl-移向右室
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上期中化學試卷(解析版) 題型:選擇題
ClO2是一種廣譜型的消毒劑,根據世界環保聯盟的要求ClO2將逐漸取代Cl2成為生產自來水的消毒劑。工業上ClO2常用NaClO3和Na2SO3溶液混合并加H2SO4酸化后反應制得,在以上反應中NaClO3和Na2SO3的物質的量之比為
A.1︰1 B. 2︰1 C. 1︰2 D. 2︰3
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 苯甲酸甲酯是一種重要的工業原料,某化學小組采用如圖裝置,以苯甲酸、甲醇為原料制取苯甲酸甲酯,有關物質的物理性質見表:
苯甲酸甲酯是一種重要的工業原料,某化學小組采用如圖裝置,以苯甲酸、甲醇為原料制取苯甲酸甲酯,有關物質的物理性質見表:| 苯甲酸 | 甲醇 | 苯甲酸甲酯 | |
| 熔點/℃ | 122.4 | -97 | -12.3 |
| 沸點/℃ | 249 | 64.3 | 199.6 |
| 濃度/g•cm3 | 1.2659 | 0.792 | 1.0888 |
| 水溶性 | 微溶 | 互溶 | 不溶 |

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
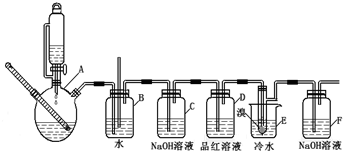
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度/g/cm3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com