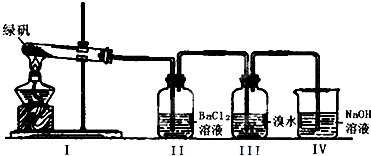
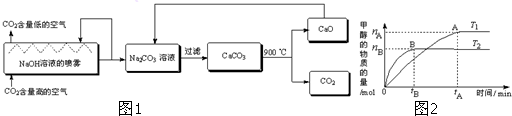
菠菜中含有一定量的草酸(HOOC-COOH)及草酸亞鐵,現通過實驗探究草酸和草酸亞鐵的性質.
Ⅰ.探究草酸的性質
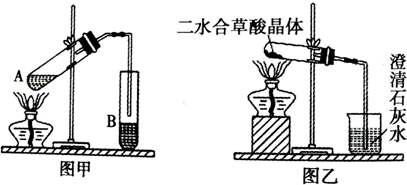
(1)向圖甲裝置的A試管加入3mL乙醇,然后邊震蕩試管邊加入2mL濃硫酸和2mL草酸,按圖甲鏈接好裝置,加熱3~5分鐘,在B試管中有油狀液體產生.該現象說明了反應(填有機反應類型)
.導管口在B試管液面上側附近的原因
.
(2)已知草酸分解的化學方程式為H
2C
2O
4H
2O+CO
2↑+CO↑.
通常情況下草酸是以二水合草酸晶體(熔點:101.5℃)的形式存在,現用乙裝置加熱二水合草酸晶體,驗證草酸的受熱分解產物,但有同學認為該裝置不合理.請你根據題給的某些物理常數和試驗目的,指出不合理的原因
、
; (回答兩條即可)
Ⅱ.探究草酸亞鐵的熱分解規律
將1.000克固體FeC
2O
4?2H
2O放在一個可稱量的容器中加熱灼燒,固體質量隨溫度升高而變化,測得數據如下表:
| 溫度/℃ | 25 | 300 | 350 | 400 | 500 | 600 | 900 |
| 固體質量/g | 1.000 | 0.800 | 0.800 | 0.400 | 0.444 | 0.444 | 0.429 |
(1)寫出25~300℃時,固體發生變化的化學方程式
.
(2)500℃時,產物中氧元素的質量分數為
.
(3)寫出600~900℃時,發生變化的化學方程式
.