
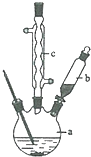
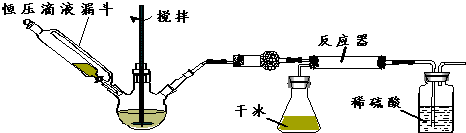
 苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線:
苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線: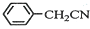 +H2O+H2SO4$\stackrel{100~130℃}{→}$
+H2O+H2SO4$\stackrel{100~130℃}{→}$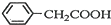 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→(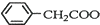 )2Cu+H2O
)2Cu+H2O分析 (1)配制此硫酸時,應將密度大的注入密度小的液體中,防止混合時放出熱使液滴飛濺;
(2)由圖可知,c為冷凝管,使氣化的液體冷凝回流,儀器b可加入反應液;反應結束后加適量冷水,降低溫度,減小苯乙酸的溶解度;分離苯乙酸粗品,利用過濾操作;
(3)苯乙酸微溶于冷水,在水中的溶解度較小;由反應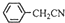 +H2O+H2SO4 $\stackrel{100-130°C}{→}$
+H2O+H2SO4 $\stackrel{100-130°C}{→}$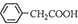 +NH4HSO4可知,40g苯乙腈生成苯乙酸為40g×$\frac{136}{117}$=46.5g;
+NH4HSO4可知,40g苯乙腈生成苯乙酸為40g×$\frac{136}{117}$=46.5g;
(4)用蒸餾水洗滌沉淀,將氯離子洗滌干凈,利用硝酸銀檢驗洗滌液確定是否洗滌干凈;
(5)苯乙酸微溶于冷水,溶于乙醇,混合溶劑中乙醇可增大苯乙酸的溶解度.
解答 解:(1)稀釋濃硫酸放出大量的熱,配制此硫酸時,應將密度大的注入密度小的液體中,防止混合時放出熱使液滴飛濺,則加入蒸餾水與濃硫酸的先后順序是先加水、再加入濃硫酸,
故答案為:先加水、再加入濃硫酸;
(2)由圖可知,c為球形冷凝管,其作用為回流(或使氣化的反應液冷凝),儀器b的作用為滴加苯乙腈;反應結束后加適量冷水,降低溫度,減小苯乙酸的溶解度,則加入冷水可便于苯乙酸析出;分離苯乙酸粗品,利用過濾操作,則需要的儀器為漏斗、燒杯、玻璃棒,
故答案為:滴加苯乙腈;球形冷凝管;回流(或使氣化的反應液冷凝);便于苯乙酸析出;BCE;
(3)苯乙酸微溶于冷水,在水中的溶解度較小,則提純苯乙酸的方法是重結晶;由反應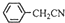 +H2O+H2SO4 $\stackrel{100-130°C}{→}$
+H2O+H2SO4 $\stackrel{100-130°C}{→}$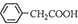 +NH4HSO4可知,40g苯乙腈生成苯乙酸為40g×$\frac{136}{117}$=46.5g,最終得到44g純品,則苯乙酸的產率是$\frac{44g}{46.5g}$×100%=95%,
+NH4HSO4可知,40g苯乙腈生成苯乙酸為40g×$\frac{136}{117}$=46.5g,最終得到44g純品,則苯乙酸的產率是$\frac{44g}{46.5g}$×100%=95%,
故答案為:重結晶;95%;
(4)用蒸餾水洗滌沉淀,將氯離子洗滌干凈,利用硝酸銀檢驗洗滌液確定是否洗滌干凈,則沉淀洗干凈的實驗操作和現象是取最后一次少量洗滌液,加入稀硝酸,再加入AgNO3溶液,無白色渾濁出現,
故答案為:取最后一次少量洗滌液,加入稀硝酸,再加入AgNO3溶液,無白色渾濁出現;
(5)苯乙酸微溶于冷水,溶于乙醇,混合溶劑中乙醇可增大苯乙酸的溶解度,然后與Cu(OH)2反應除去苯乙酸,即混合溶劑中乙醇的作用是增大苯乙酸溶解度,便于充分反應,
故答案為:增大苯乙酸溶解度,便于充分反應.
點評 本題考查苯乙酸銅的合成,側重物質制備實驗及有機物性質的考查,把握合成反應及實驗裝置的作用為解答的關鍵,綜合考查學生實驗技能和分析解答問題的能力,題目難度中等,注意信息的處理及應用.


科目:高中化學 來源: 題型:選擇題
| A. | “水乳交融,火上澆油”前者包含物理變化,后者包含化學變化 | |
| B. | “滴水石穿.繩鋸木斷”不包含化學變化 | |
| C. | “蠟炬成灰淚始干”包含的是物理變化 | |
| D. | 石灰吟中“烈火焚燒若等閑”指的是加熱,不包含化學變化 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
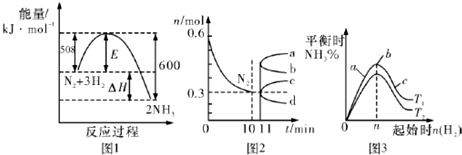
| A. | 升高溫度,該反應的平衡常數增大 | |
| B. | 由圖2信息,10 min內該反應的平均速率v(H2)=0.09 mol•L-1•min-1 | |
| C. | 由圖2信息,從11 min起其它條件不變,壓縮容器的體積,則n(N2)的變化曲線為d | |
| D. | 圖3中溫度T1<T2,a、b、c三點所處的平衡狀態中,反應物N2的轉化率最高的是b點 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
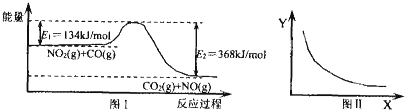
| A. | 該反應的焓變△H=+234 kJ•mol-1 | |
| B. | 若X表示溫度,則Y表示的可能是CO2的物質的量濃度 | |
| C. | 若X表示CO的起始濃度,則Y表示的可能是NO2的轉化率 | |
| D. | 若X表示反應時間,則Y表示的可能是混合氣體的密度 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
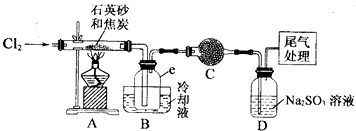
| 物質 | SiC14 | A1C13 | FeC13 |
| 沸點/℃ | 57.7 | - | 315 |
| 熔點/℃ | -70.0 | - | - |
| 升華溫度/℃ | - | 180 | 300 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
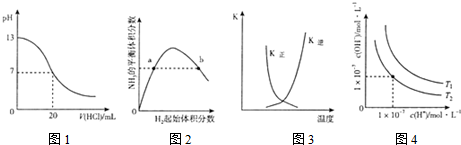
| A. | 圖1表示25℃時,用0.lmol L-1鹽酸滴定20mL 0.1mol•L-1NaOH溶液,溶液的pH隨加入酸體積的變化 | |
| B. | 圖2表示一定條件下的合成氨反應中.NH3的平衡體積分數隨H2起始體積分數(N2的起始量恒定)的變化,圖中a點N2的轉化率大于b點 | |
| C. | 圖3表示恒容密閉容器中反應“2SO2(g)+O2(g)?2SO3(g)△H<0”的平衡常數K正、K逆隨溫度的變化 | |
| D. | 圖4表示不同溫度下水溶液中H+和OH-濃度的變化的曲線,圖中溫度T2>T1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
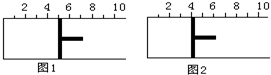 如圖所示,一定條件下將lmolA氣體和3molB氣體充入一個體積可變的密閉容器中,可滑動活塞的位置圖1所示.在恒溫恒壓下發生A(g)+3B(g)?2C(g),當反應達到平衡時,活塞位置如圖2所示,則平衡時A的轉化率為( )
如圖所示,一定條件下將lmolA氣體和3molB氣體充入一個體積可變的密閉容器中,可滑動活塞的位置圖1所示.在恒溫恒壓下發生A(g)+3B(g)?2C(g),當反應達到平衡時,活塞位置如圖2所示,則平衡時A的轉化率為( )| A. | 20% | B. | 40% | C. | 50% | D. | 無法確定 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com