
分析 (1)2NH3(g)+CO2(g)?NH2COONH4(s),該反應為熵減的過程,若能自發進行,說明該反應為放熱反應,據此解答即可;
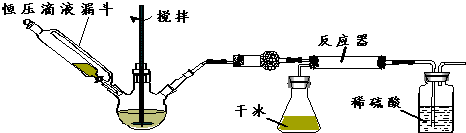
(2)恒壓滴液漏斗代替分液漏斗可以平衡內外壓強,使氨水順利滴下;
(3)反應物氨氣必須是干燥的,需要用堿性干燥劑干燥,如堿石灰、固體氫氧化鈉或氧化鈣等;
(4)濃氨水加入氫氧化鈉固體,氫氧化鈉固體溶解放熱,使一水合氨分解生成氨氣的化學平衡NH3+H2O?NH3•H2O?NH4++OH-,逆向進行;
(5)干冰制取的二氧化碳中不含雜質,不需要干燥;該反應為放熱反應,干冰變為二氧化碳吸收熱量,有利于增大反應物轉化率;
(6)反應后期二氧化碳的量減少,可以采取措施讓通入的氨氣也減少;
(7)依據裝置圖中流程分析,安全問題主要是堵塞導氣管,液體發生倒吸;依據反應過程中的產物分析,不能把污染性的氣體排放到空氣中,吸收易溶于水的氣體需要放倒吸.
解答 解:(1)2NH3(g)+CO2(g)?NH2COONH4(s),該反應為熵減的過程,若能自發進行,說明該反應為放熱反應,即△H<0,
故答案為:小于;
(2)和普通分液漏斗相比,恒壓滴液漏斗上部和三頸燒瓶氣壓相通,可以保證恒壓滴液漏斗中的液體順利滴下,
故答案為:使氨水順利滴下;
(3)由于制備氨基甲酸銨的原料氨氣必須是干燥的,以防止副反應的發生,因此生成的氨氣必須進行干燥,因為氨氣是堿性氣體,所以干燥氨氣應該用氧化鈣或固體氫氧化鈉或堿石灰,
故答案為:固體氫氧化鈉或堿石灰;
(4)濃氨水加入氫氧化鈉固體,氫氧化鈉固體溶解放熱,使一水合氨分解生成氨氣的化學平衡NH3+H2O?NH3•H2O?NH4++OH-,逆向進行,能用化學平衡移動原理解釋,
故答案為:氫氧化鈉固體溶解放熱和OH-使一水合氨分解生成氨氣的化學平衡NH3+H2O?NH3•H2O?NH4++OH-逆向進行.
(5)碳酸鹽和酸反應制CO2,則生成的CO2必須進行凈化和干燥處理,而直接利用干冰制備CO2,不需要干燥;又因為該反應是放熱反應,提供低溫環境,可以提高轉化率,
故答案為:不需要干燥;提供低溫環境,提高轉化率;
(6)反應后期,由于二氧化碳的氣流下降,導致通入的二氧化碳氣體減少,此時可以通過調節恒壓滴液漏斗旋塞,減慢氨水的滴加速度,
故答案為:調節恒壓滴液漏斗旋塞,減慢氨水的滴加速度;
(7)依據裝置圖中流程分析,安全問題主要是堵塞導氣管,液體發生倒吸;依據反應過程中的產物分析,不能把污染性的氣體排放到空氣中,吸收易溶于水的氣體需要放倒吸,實驗裝置存在安全問題產品易堵塞導管,稀硫酸會倒吸,
故答案為:產品易堵塞導管,稀硫酸會倒吸.
點評 本題考查了物質制備實驗的設計應用,主要是氨氣的制備方法,氨基甲酸的制備實驗裝置分析判斷,實驗基本操作,混合物分離的實驗設計,題目難度中等.


科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
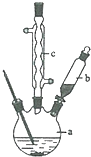 苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線:
苯乙酸銅是合成優良催化劑、傳感材料--納米氧化銅的重要前驅體之一.下面是它的一種實驗室合成路線: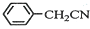 +H2O+H2SO4$\stackrel{100~130℃}{→}$
+H2O+H2SO4$\stackrel{100~130℃}{→}$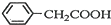 +NH4HSO4
+NH4HSO4 +Cu(OH)2→(
+Cu(OH)2→(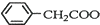 )2Cu+H2O
)2Cu+H2O查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
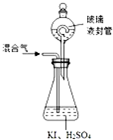 二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑,回答下列問題:
二氧化氯(ClO2,黃綠色易溶于水的氣體)是高效、低毒的消毒劑,回答下列問題: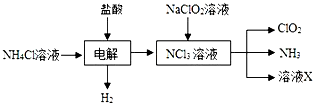
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=($\frac{10Q}{9}$-1366.8)kJ•mol-1 | |
| B. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=(-$\frac{10Q}{9}$+1366.8)kJ•mol-1 | |
| C. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=($\frac{10Q}{9}$-151.9)kJ•mol-1 | |
| D. | CxHy(l)+(x+$\frac{y}{4}$)O2(g)=xCO2(g)+$\frac{y}{2}$H2O(l)△H=(-$\frac{10Q}{9}$+151.9)kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
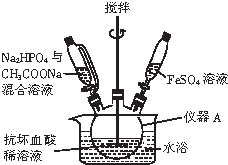 磷酸亞鐵晶體[Fe3(PO4)2•8H2O]是藍白色單斜晶體,溶于稀強酸,不溶于水、醋酸、醇,主要用于制作磷酸鐵銼電池.實驗室制備磷酸亞鐵晶體的裝置、反應原理和實驗步驟如下:
磷酸亞鐵晶體[Fe3(PO4)2•8H2O]是藍白色單斜晶體,溶于稀強酸,不溶于水、醋酸、醇,主要用于制作磷酸鐵銼電池.實驗室制備磷酸亞鐵晶體的裝置、反應原理和實驗步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 銣比鎂金屬性強 | |
| B. | 氯化鎂比氯化銣難溶 | |
| C. | 高溫下,鎂離子得電子能力比銣離子弱 | |
| D. | 銣的沸點比鎂低,當把銣蒸氣抽走時,平衡向右反應方向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(g)△H=-48.4 kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-5517.6 kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=+5517.6 kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)═8CO2(g)+9H2O(l)△H=-48.4 kJ•mol-1 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com