
| 編號 | 操作 | 現象等 |
| Ⅰ | 先向2mL 0.1mol/L FeC12溶液中滴加KSCN溶液,再滴加新制氯水 | ①滴加KSCN溶液后,溶液無明顯變化;滴加新制氯水后,溶液變變成紅色 ②FeC12溶液與新制氯水反應的離子方程式2Fe2++Cl2═2Fe3++2Cl- |
| Ⅱ | 先向2mL 0.1mol/L FeC13溶液中滴加KSCN溶液,再滴加0.1mol/L KI溶液 | 滴加KSCN溶液后,溶液變紅色;滴加KI溶液后,紅色無明顯變化 |
| 編號 | 操作 | 現象等 |
| Ⅲ | 先向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeC13溶液,再滴加KSCN溶液 | 滴加FeC13溶液后,溶液變成黃色;滴加KSCN溶液后,溶液變為紅色.根據實驗現象可以推測出Fe3+有可能與I-發生了氧化還原反應. |
| 編號 | 操作 | 現象及結論 |
| Ⅳ | 向2mL 0.1mol/L KI溶液中滴加1mL 0.1mol/L FeC13溶液,再滴加①再滴加淀粉溶液(或CCl4;或鐵氰化鉀溶液) | 現象:溶液變藍. 結論:Fe3+能與I-發生氧化還原反應生成②I2,③Fe2+ |
分析 (1)Ⅰ.亞鐵離子和硫氰化鉀溶液不反應,但亞鐵離子有還原性,能被氯氣氧化生成鐵離子,鐵離子和硫氰根離子反應生成血紅色的絡合物,導致溶液呈血紅色;
(2)碘水溶液呈黃色,生成了碘單質,說明發生了氧化還原反應;
(3)碘離子和鐵離子發生氧化還原反應且參加反應的Fe3+與I-的物質的量相同,再結合得失電子數相等確定反應方程式;
(4)如果碘離子和鐵離子反應生成亞鐵離子和碘單質,根據亞鐵離子的特征反應或碘單質的特征反應進行實驗,碘遇淀粉溶液變藍色、碘溶于四氯化碳后溶液呈紫色,亞鐵離子和鐵氰化鉀溶液反應生成藍色沉淀.
解答 解:(1)Ⅰ.①亞鐵離子和硫氰化鉀溶液不反應,所以向氯化亞鐵溶液中滴加硫氰化鉀溶液后,溶液不呈紅色,再滴加氯水后,氯氣把亞鐵離子氧化呈鐵離子,鐵離子和硫氰化鉀溶液反應生成絡合物,導致溶液呈血紅色,所以實驗I的現象為滴加KSCN后溶液無明顯變化,加入氯水后溶液變成紅色,
故答案為:無明顯變化;變成紅色;
②氯化亞鐵和氯氣反應生成氯化鐵,離子方程式為:2Fe2++Cl2═2Fe3++2Cl-,
故答案為:2Fe2++Cl2═2Fe3++2Cl-;
(2)碘水溶液呈黃色,根據溶液變成黃色,推測生成了I2,說明發生了氧化還原反應,
故答案為:氧化還原;
(3)Fe3+與I-發生氧化還原反應,且參加反應的Fe3+與I-的物質的量相同,所以該反應的離子方程式為:2Fe3++2I-?2Fe2++I2,
故答案為:2Fe3++2I-?2Fe2++I2;
(4)如果碘離子和鐵離子發生氧化還原反應生成碘單質和亞鐵離子,亞鐵離子和鐵氰化鉀溶液反應生成藍色沉淀,碘單質遇淀粉溶液變藍色,碘溶于四氯化碳后溶液呈紫色,所以如果要檢驗碘單質和亞鐵離子,可以用再滴加淀粉溶液(或CCl4;或鐵氰化鉀溶液)檢驗,
反應現象為:溶液變藍(或溶液分層,下層溶液為紫色;或生成藍色沉淀),
得出結論為:Fe3+能與I-發生氧化還原反應,生成I2(或Fe2+),
故答案為:
| 編號 | 操作 | 預期現象及結論 |
| IV | 再滴加淀粉溶液(或CCl4;或鐵氰化鉀溶液) | I2;Fe2+ |
點評 本題考查了性質實驗方案的設計與評價,題目難度中等,明確鐵離子和亞鐵離子的性質及檢驗方法為解答關鍵,注意掌握實驗方案設計與評價的原則,試題培養了學生的分析能力及化學實驗能力.


科目:高中化學 來源: 題型:選擇題
| A. | 甲苯苯環上的一個氫原子被-C3H7的烷基取代 | |
| B. | C5H12被C12取代生成的一氯代物 | |
| C. | 與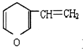 互為同分異構體的芳香族化合物 互為同分異構體的芳香族化合物 | |
| D. | 菲( 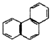 )的一硝基取代物 )的一硝基取代物 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 熱化學方程式:H2(g)+F2(g)=2HF(g)△H=-270 kJ,表示的意義為2 L氟化氫氣體分解成1 L氫氣與1 L氟氣吸收270 kJ熱量 | |
| B. | 用pH試紙測定1 mol/L的醋酸溶液,顯示的pH為2~3能證明醋酸為弱電解質 | |
| C. | 為減少洗滌過程中固體的損失,最好選用稀H2SO4代替H2O來洗滌BaSO4沉淀 | |
| D. | pH計是精確測定溶液pH的儀器 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 碳酸氫鈉俗稱蘇打 | |
| B. | 鑒別Na2CO3和NaHCO3兩種無色溶液,可以分別滴加Ba(OH)2溶液,觀察有無白色沉淀 | |
| C. | NaHCO3的熱穩定性大于Na2CO3 | |
| D. | 向滴有酚酞試劑的水中加入足量的Na2O2粉末并振蕩,溶液由無色變紅最后又變無色 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 放熱反應在常溫下均能自發進行 | |
| B. | 原電池工作時所發生的反應一定有氧化還原反應 | |
| C. | 加熱時,化學反應只向吸熱反應方向進行 | |
| D. | 化學平衡常數的表達式與化學反應方程式的書寫無關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 可用水來鑒別苯和CCl4 | |
| B. | 煤的干餾屬于化學變化,硝化反應、酯化反應、皂化反應都屬于取代反應 | |
| C. | CH2Cl2有兩種同分異構體 | |
| D. | 高溫加熱能殺死病毒是因為構成病毒的蛋白質受熱變性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室中常用飽和食鹽水除去Cl2中混有的HCl | |
| B. | 銀器長期放置,表面變暗 | |
| C. | 紅棕色的NO2加壓后顏色先變深再變淺 | |
| D. | 氨水中加酸,NH4+的濃度增大 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com