
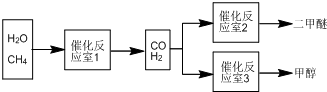
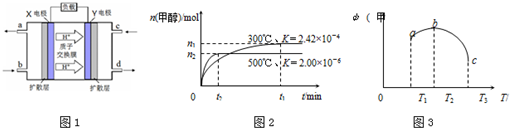
分析 (1)10min內反應的平均速率v(CO)=$\frac{\frac{△n}{V}}{△t}$,v(H2)=3v(CO);該反應平衡常數K等于生成物濃度冪之積與反應物濃度冪之積的比;
(2)CH3OCH3 (g)+3O2(g)=2 CO2(g)+3H2O(g)△H=-1323KJ/mol①;
2H2(g)+O2(g)═2H2O(g)△H=-484KJ/mol②;
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)H=-283KJ/mol③,
將方程式2②+2③-①得2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g),焓變進行相應的改變;
(3)根據氫離子移動方向知,X是負極、Y是正極,該原電池是燃料電池,則X電極上二甲醚失電子發生氧化反應、Y電極上氧氣得電子發生還原反應,X電極上二甲醚失電子生成二氧化碳和氫離子;
(4)①升高溫度平衡向吸熱方向移動,根據甲醇的物質的量多少判斷焓變;
②A.溫度越高化學反應速率越快;
B.該反應的正反應是放熱反應,升高溫度平衡逆向移動;
C.該反應的正反應是放熱反應,升高溫度平衡逆向移動,溫度由T1到T2平衡正向移動,由T2到T3平衡逆向移動;
D.該反應為放熱反應,升高溫度,平衡逆向移動;反應后氣體體積小于反應前,減小壓強.平衡逆向移動.
解答 解:(1)10min內反應的平均速率v(CO)=$\frac{\frac{△n}{V}}{△t}$=$\frac{\frac{0.1mol}{10L}}{10min}$=0.001mol/(L.min),v(H2)=3v(CO)=0.003mol/(L.min);該反應平衡常數K等于生成物濃度冪之積與反應物濃度冪之積的比,所以該反應化學平衡常數K=$\frac{c(CO).{c}^{3}({H}_{2})}{c(C{H}_{4}).c({H}_{2}O)}$,
故答案為:0.003mol/(L.min);K=$\frac{c(CO).{c}^{3}({H}_{2})}{c(C{H}_{4}).c({H}_{2}O)}$;
(2)CH3OCH3 (g)+3O2(g)=2 CO2(g)+3H2O(g)△H=-1323KJ/mol①;
2H2(g)+O2(g)═2H2O(g)△H=-484KJ/mol ②;
CO(g)+$\frac{1}{2}$O2(g)═CO2(g)H=-283KJ/mol③,
將方程式2②+2③-①得2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g),△H=2×(-484kJ/mol)+2×(-283kJ/mol)-(-1323kJ/mol)=-211kJ/mol,
故答案為:2CO(g)+4H2(g)═CH3OCH3(g)+H2O(g)△H=-211kJ/mol;
(3)根據氫離子移動方向知,X是負極、Y是正極,該原電池是燃料電池,則X電極上二甲醚失電子發生氧化反應、Y電極上氧氣得電子發生還原反應,X電極上二甲醚失電子生成二氧化碳和氫離子,電極反應式為(CH3)2O-12e-+3H2O=2CO2+12H+,
故答案為:(CH3)2O-12e-+3H2O=2CO2+12H+;
(4)①升高溫度平衡向吸熱方向移動,根據圖知,升高溫度甲醇體積分數降低,說明平衡逆向移動,則正反應是放熱反應,焓變小于0,故答案為:<;
②A.溫度越高化學反應速率越快,溫度T1<T2<T3,所以反應速率a<b<c,故A錯誤;
B.該反應的正反應是放熱反應,升高溫度平衡逆向移動,溫度T1<T2<T3,所以CO轉化率a>b>c,故B正確;
C.該反應的正反應是放熱反應,升高溫度平衡逆向移動,溫度由T1到T2平衡正向移動,由T2到T3平衡逆向移動,所以a未達到平衡狀態,b可能達到平衡狀態,c達到平衡狀態,故C錯誤;
D.該反應為放熱反應,升高溫度,平衡逆向移動;反應后氣體體積小于反應前,減小壓強.平衡逆向移動,故將容器b中的平衡狀態轉變到容器c中的平衡狀態,可采取的措施有升溫或減壓,故D正確,
故答案為:BD.
點評 本題考查化學平衡計算、原電池原理等知識點,側重考查學生圖象分析判斷及計算能力,難點是電極反應式的書寫及(4)圖象分析,易錯點是(4)②中C平衡點判斷,題目難度中等.


科目:高中化學 來源: 題型:解答題

 .
.查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
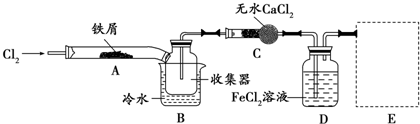
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C2H5OH(l)+3O2(g)═2CO2(g)+3H2O(g)△H=-1367.0 kJ/mol (燃燒熱) | |
| B. | 已知C(石墨,s)═C(金剛石,s)△H>0,則金剛石比石墨穩定 | |
| C. | S(s)+O2(g)═SO2(g)△H=-296.8 kJ/mol (反應熱) | |
| D. | 已知2C(s)+2O2(g)═2CO2(g)△H1;2C(s)+O2(g)═2CO(g)△H2,則△H1>△H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
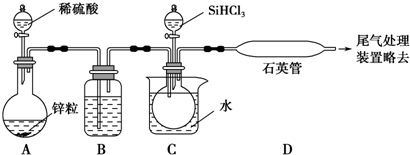
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3△H1+2△H2-△H3 | B. | △H1+△H2-△H3 | C. | 3△H1+△H2+△H3 | D. | 3△H1+△H2-△H3 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 化學鍵 | H-H | N三N | N-H |
| 鍵能/(kJ•mol-1) | 436 | 945.6 | 391 |
| A. | +192.4 kJ•mol-1 | B. | +92.4kJ•mol-1 | C. | -92.4kJ•mol-1 | D. | -192.4kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
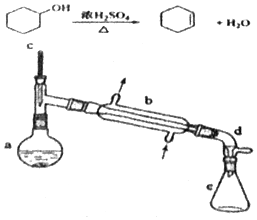 分離提純是化學實驗中的重要部分,方法有過濾、蒸發、萃取、蒸餾等,應用廣泛,環己醇 脫水是合成環己烯的常用方法,實驗室合成壞己烯的反應和實驗裝置如圖:
分離提純是化學實驗中的重要部分,方法有過濾、蒸發、萃取、蒸餾等,應用廣泛,環己醇 脫水是合成環己烯的常用方法,實驗室合成壞己烯的反應和實驗裝置如圖:| 相對分子質量 | 密度/(g•cm-3) | 沸點/℃ | 溶解性 | |
| 環己醇 | 100 | 0.9618 | 161 | 微溶于水 |
| 環己烯 | 82 | 0.8102 | 83 | 難溶于水 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com