
分析 (1)鐵離子水解生成氫氧化鐵和氫離子,溶液呈酸性;
(2)依據反應Fe3++Ag?Fe2++Ag+,分析判斷氯離子不變,鐵元素質量不變;
(3)硝酸根離子在酸溶液中具有氧化性,可以氧化銀、亞鐵離子;
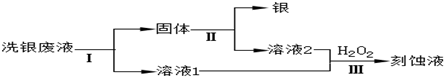
(4)①洗銀廢液(Fe3+、Fe2+、Ag+、NO3-)中回收銀和刻蝕液需要先加入過量鐵還原Fe3+、Ag+;
②試劑Ⅱ是溶解過量的鐵;
(5)①銀氨溶液中加入過量鹽酸生成氯化銀;
②向沉淀AgCl中加入羥氨(NH2OH),充分反應后可得銀,羥氨被氧化為N2.反應為:2AgCl+2NH2OH=N2↑+2Ag+2H2O+2HCl,依據反應計算.
解答 解:(1)FeCl3溶液顯酸性是因為鐵離子水解生成氫氧化鐵和氫離子;反應的離子方程式為:Fe3++3H2O?Fe(OH)3+3H+;
故答案為:Fe3++3H2O?Fe(OH)3+3H+;
(2)FeCl3溶液洗銀,發生反應為:Fe3++Ag?Fe2++Ag+,
a.c(Fe3+)減小,故a符合;
b. c(Cl-)改變,故b不符合;
c.鐵元素存在形式不同但質量不會減小,故c不符合;
故答案為:a;
(3)通過檢驗Fe(NO3)3溶液洗銀后NO3-的還原產物來判斷NO3-是否能將銀氧化,需要在酸溶液中,亞鐵離子也會反應,則該方法不可行;
故答案為:不可行;酸性條件下NO3-也可能與Fe2+發生氧化還原反應;
(4)①洗銀廢液(Fe3+、Fe2+、Ag+、NO3-)中回收銀和刻蝕液需要先加入過量鐵還原Fe3+、Ag+;反應的離子方程式為:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
故答案為:2Fe3++Fe=3Fe2+,Fe+2Ag+=Fe2++2Ag;
②過程Ⅱ中加入的試劑是溶解過量的鐵,可以用稀鹽酸或稀硫酸;
故答案為:稀鹽酸或稀硫酸;
(5)①銀氨溶液中加入過量鹽酸生成氯化銀,同時生成氯化銨和水,反應的化學方程式為:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;
故答案為:Ag(NH3)2OH+3HCl=AgCl↓+2NH4Cl+H2O;
②向沉淀AgCl中加入羥氨(NH2OH),充分反應后可得銀,羥氨被氧化為N2.反應為:2AgCl+2NH2OH=N2↑+2Ag+2H2O+2HCl,反應中消耗3.3g羥氨物質的量=$\frac{3.3g}{33g/mol}$=0.1mol;生成銀物質的量為0.1mol,質量為10.8g;
故答案為:10.8.
點評 本題考查物質的性質實驗,為高頻考點,側重于學生的分析、實驗能力的考查,題目注重回收利用的提取過程鹽類分析判斷,試劑選擇的目的,離子方程式化學方程式書寫的方法,掌握物質性質是關鍵,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 當消耗0.1 mol Zn時,得到的還原產物為0.1 mol | |
| B. | 當溶液中不再產生氣泡時,溶液中大量存在的陽離子是Zn2+ | |
| C. | 當有第三種單質生成時,消耗的鋅粉質量至少大于13 g | |
| D. | 反應結束時,可得到0.25 mol ZnSO4 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 與足量的氫氣和新制備的氫氧化銅反應,消耗的氫氣與氫氧化銅的量分別為( )
與足量的氫氣和新制備的氫氧化銅反應,消耗的氫氣與氫氧化銅的量分別為( )| A. | 1 mol、2 mol | B. | 1 mol、4 mol | C. | 3 mol、2 mol | D. | 3 mol、4 mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁是地殼中含量最多的金屬元素,在生活中有廣泛的應用,但鋁制品不宜長時間盛放腌制食品 | |
| B. | 世博停車場安裝催化光解設施,可將汽車尾氣中的CO和NOX反應生成無毒物質 | |
| C. | 綠色化學的核心是應用化學原理對環境污染進行治理 | |
| D. | 高容量的儲氫材料研究是推廣應用氫氧燃料電池的關鍵問題之一 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向漂白液中通入少量二氧化碳:ClO-+H2O+CO2═${CO}_{3}^{2-}$+2HClO | |
| B. | 常溫時偏鋁酸鈉溶液pH>7:${AlO}_{2}^{-}$+2H2O═Al(OH)3↓+OH- | |
| C. | 等物質的量濃度的FeI2溶液與溴水等體積混合:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| D. | 向硫酸氫鈉溶液中滴加Ba(OH)2溶液恰好至沉淀完全:H++${SO}_{4}^{2-}$+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{125a}{72V}$ mol•L-1 | B. | $\frac{125a}{36V}$ mol•L-1 | C. | $\frac{250a}{36V}$ mol•L-1 | D. | $\frac{250a}{48V}$ mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com