
| A. | 二氧化硅溶于水顯酸性 | |
| B. | 二氧化碳通入水玻璃(Na2SiO3的水溶液)可以得到白色膠狀物質 | |
| C. | 因為高溫時,二氧化硅與碳酸鈉反應放出二氧化碳,所以硅酸的酸性比碳酸強 | |
| D. | 二氧化硅是酸性氧化物,它不溶于任何酸 |
分析 A.二氧化硅屬于酸性氧化物但和水不反應;
B.碳酸酸性大于硅酸,所以二氧化碳、水和硅酸鈉反應生成原硅酸;
C.高溫下,二氧化硅與碳酸鈉反應放出二氧化碳,不能據此判斷硅酸和碳酸的相對強弱;
D.二氧化硅屬于酸性氧化物,但能溶于HF.
解答 解:A.二氧化硅屬于酸性氧化物但和水不反應,用二氧化硅和NaOH溶液制取硅酸鈉,然后用硅酸鈉制取硅酸,故A錯誤;
B.碳酸酸性大于硅酸,所以二氧化碳、水和硅酸鈉反應生成原硅酸,故B正確;
C.高溫下,二氧化硅與碳酸鈉反應放出二氧化碳,因為有高溫條件,所以不能據此判斷硅酸和碳酸的相對強弱,故C錯誤;
D.二氧化硅屬于酸性氧化物,能溶于強堿溶液,且能溶于HF,所以可以用HF雕刻玻璃,故D錯誤;
故選B.
點評 本題考查二氧化硅的性質,二氧化硅屬于酸性氧化物但能溶于HF,知道制取硅酸的方法,題目難度不大.


科目:高中化學 來源: 題型:解答題
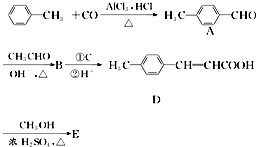
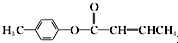 是E的一種同分異構體,該物質與足量NaOH溶液共熱的化學方程式為
是E的一種同分異構體,該物質與足量NaOH溶液共熱的化學方程式為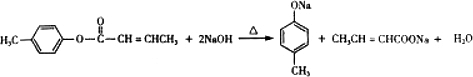 .
.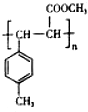 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3COONa的溶液:CH3COO-+H2O═CH3COOH+OH- | |
| B. | NH4Cl的溶液:NH4++H2O?NH3•H2O+H+ | |
| C. | Na2CO3的溶液:CO32-+H2O?H2CO3+2OH- | |
| D. | AlCl3的溶液:Al3++3H2O═Al(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
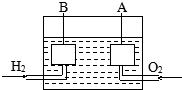 宇宙飛船上使用的氫氧燃料電池是一種新型化學電池,其構造如圖所示,A、B是多孔性炭制成的兩個電極,通入的氣體由孔隙中逸出,并在電極表面放電.
宇宙飛船上使用的氫氧燃料電池是一種新型化學電池,其構造如圖所示,A、B是多孔性炭制成的兩個電極,通入的氣體由孔隙中逸出,并在電極表面放電.查看答案和解析>>
科目:高中化學 來源: 題型:填空題

 (1)FeCl3具有凈水作用,但腐蝕設備,FeCl3溶液腐蝕鋼鐵設備,除H+作用外,另一主要原因是(用離子方程式表示)2Fe3++Fe=3Fe2+.
(1)FeCl3具有凈水作用,但腐蝕設備,FeCl3溶液腐蝕鋼鐵設備,除H+作用外,另一主要原因是(用離子方程式表示)2Fe3++Fe=3Fe2+.
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 室溫下c(NH4+)相同的下列溶液:①NH4Al(SO4)2②NH4Cl③CH3COONH4,物質的量濃度由大到小的順序為②>①>③ | |
| B. | 0.001mol•L-1氯水中:c(Cl2)+c(Cl-)+c(ClO-)+c(HClO)=0.01mol•L-1 | |
| C. | amol•L-1的醋酸與0.01mol•L-1的氫氧化鈉溶液等體積混合后呈中性,則醋酸的Ka=5×10-10/(a/2-0.005) | |
| D. | 向5mL含KCl和Kl濃度均為0.01mol•L-1的混合溶液中,滴加8mL0.01mol•L-1的AgNO3溶液,所得溶液中離子濃度大小關系為c(NO3-)>c(K+)>c(Cl-)>c(I-)>c(Ag+) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com