
| 元素 | X | Y | Z | W |
| 相關信息 | 短周期p區元素,有種單質常作電極材料 | 基態原子2p能級上各軌道中均有電子且電子的自旋方向相同 | 基態原子的核外電子共有17種運動狀態 | 位于第四周期第VA族 |
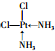 (YH3作為一個整體寫)
(YH3作為一個整體寫)
分析 X為短周期p區元素,有種單質常作電極材料,則X為C元素;Y的基態原子2p能級上各軌道中均有電子且電子的自旋方向相同,則Y的2p軌道含有3個電子,為N元素;Z基態原子的核外電子共有17種運動狀態,其原子的核外電子總數17,則Z為Cl元素;W位于第四周期第VA族,則W為As元素,據此結合元素周期律知識進行解答.
解答 解:X為短周期p區元素,有種單質常作電極材料,則X為C元素;Y的基態原子2p能級上各軌道中均有電子且電子的自旋方向相同,則Y的2p軌道含有3個電子,為N元素;Z基態原子的核外電子共有17種運動狀態,其原子的核外電子總數17,則Z為Cl元素;W位于第四周期第VA族,則W為As元素,
(1)As是35號元素,屬于主族元素,其最外層電子就是其價電子,所以As基態原子的價電子排布式:4s24p3;Cl的非金屬性大于As,則第一電離能大小為:Cl>As,
故答案為:4s24p3;Cl>As;
(2)Cl能與C、N、As形成CCl4、NCl3、AsCl3、AsCl5等化合物,其中CCl4形成4個C-Clσ鍵鍵,NCl3、AsCl3中含有3個σ鍵和1對孤電子對,所以它們的中心原子的雜化方式為sp3,而AsCl5中As含有5個As-Cl鍵,不是sp3雜化;其中NCl3、AsCl3為V形,分子構型為正四面體的為CCl4,
故答案為:CCl4、NCl3、AsCl3;CCl4;
(3)①Pt(YH3)2Z2為PtCl2(NH3)2,根據相似相溶原理,因為淡黃色固體Q,較難溶于極性溶劑水,則Q為非金屬性分子,
故答案為:非極性分子;
②通過相似相溶原理可知兩種固體一種為極性分子,另一種為非極性分子,若PtCl2(NH3)2為四面體結構,只能為極性分子,故只能為平面正方形結構,黃綠色(P)在水中的溶解度較大,則P為極性分子,其結構簡式為: ,
,
故答案為: ;
;
(4)X為C元素,每個原子最外層都滿足8電子穩定結構,根據圖示可知,每個C原子形成了3個鍵,則每個C形成的這3個鍵中,必然有1個雙鍵,這樣每個C原子最外層才滿足8電子穩定結構,雙鍵數應該是C原子數的一半,而雙鍵中有1個σ鍵、1個π鍵,所以分子中σ鍵與π鍵數目之比為3:1;
一定條件下含NA個C原子的N中含有C原子的物質的量為:$\frac{N}{{N}_{A}}$mol=1mol,含有碳碳雙鍵的數目為:1mol×$\frac{1}{2}$=0.5mol,0.5mol碳碳雙鍵完全反應消耗0.5mol氫氣,消耗氫氣的質量為:2g/mol×0.5mol=1g,
故答案為:3:1;1;
(5)根據化學式GaAs可知,晶胞中Ga和As的配位數相同,根據圖示可知,每個As連接了4個Ga,則Ga和As的配位數都是4;Ga原子位于立方體的頂點和面心,每個晶胞中含有Ga數目為:8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,則同時含有4個As;每個晶胞的質量為:4×$\frac{145}{{N}_{A}}$g=$\frac{580}{{N}_{A}}$g,該晶胞的密度為ρg•cm-3,則該晶胞的體積為:V=$\frac{\frac{580}{{N}_{A}}g}{ρg•c{m}^{-3}}$=$\frac{580}{ρ•{N}_{A}}$cm3,所以該晶胞的邊長為:$\root{3}{\frac{580}{ρ•{N}_{A}}}$,
故答案:4;$\root{3}{\frac{580}{ρ•{N}_{A}}}$.
點評 本題考查了位置、結構與性質關系的綜合應用,題目難度較大,注意掌握原子結構與元素周期律、元素周期表的關系,(5)為難點,注意掌握晶胞中密度、邊長的計算方法.


 輕松暑假總復習系列答案
輕松暑假總復習系列答案科目:高中化學 來源: 題型:選擇題
| A. | 光化學煙霧是氮氧化物受紫外線照射后與空氣中的一些碳氫化合物作用后生成的一種有毒煙霧 | |
| B. | 以糧食為原料釀酒過程的變化包括糧食→淀粉→葡萄糖→乙醇 | |
| C. | 航天飛機上使用的隔熱陶瓷瓦,大多是以碳纖維做增強體的新型復合材料 | |
| D. | 綠色化學的核心是應用化學原理對環境污染進行治理 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | S2-和HS- | B. | H3O+和OH- | C. | Na+和NH${\;}_{4}^{+}$ | D. | K+和Ne |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
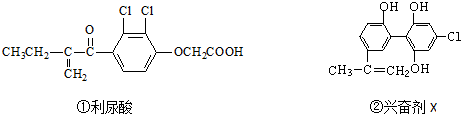
| A. | 利尿酸分子中有三種含氧官能團,在核磁共振氫譜上共有六個峰 | |
| B. | 1 mol興奮劑X與足量濃溴水反應,最多消耗4 mol Br2 | |
| C. | 兩種興奮劑最多都能和含3molNaOH的溶液反應 | |
| D. | 兩種分子中的所有碳原子均不可能共平面 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 2A(l)+B(l)=2C(l)△H1 2A (g)+B(g)=2C(l)△H2 則△H1>△H2 | |
| B. | 31g紅磷變成31g白磷要吸收能量,說明紅磷比白磷更穩定 | |
| C. | 測定HCl和NaOH的中和熱時,每次實驗均應測量三個溫度,即鹽酸的起始溫度、NaOH的起始溫度和反應結束后穩定的溫度 | |
| D. | 在101 kPa時,已知氫氣的燃燒熱為285.8kJ/mol,則氫氣燃燒的熱化學方程式表示為2H2(g)+O2(g)═2H2O(g)△H=-571.6 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 構成原電池正極和負極的材料必須是兩種金屬 | |
| B. | 由銅、鋅電極與硫酸銅溶液組成的原電池中銅是負極 | |
| C. | 電子由鋅片流經稀硫酸溶液到銅片,氫離子在銅片上得到電子放出氫氣 | |
| D. | 銅鋅原電池工作時,若有13g鋅被溶解,電路中就有0.4mol電子通過 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
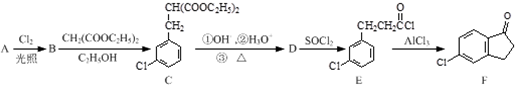
 ,反應E→F的反應類型取代反應.
,反應E→F的反應類型取代反應.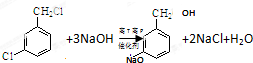 .
. 或
或 (任寫一種).
(任寫一種).
 .
.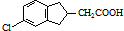 的合成路線流程圖(注明反應條件).合成路線流程圖示例如下:
的合成路線流程圖(注明反應條件).合成路線流程圖示例如下: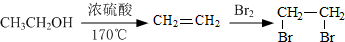
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com