

| A. | 氣體W為氧氣 | |
| B. | b極與電源的正極相連 | |
| C. | 離子交換膜c為陽離子交換膜 | |
| D. | a極的電極反應為SO2+2H2O-2e-=SO42-+4H+. |
分析 根據圖知,右邊裝置中加入較稀的NaOH溶液,電解后得到較濃的NaOH溶液,說明b電極上發生的反應為2H2O-4e-=2H2↑+4OH-,所以b是陰極、a是陽極,左邊裝置中,加入稀硫酸和SO2,電解后得到較濃的硫酸,電極反應式為SO2+2H2O-2e-=SO42-+4H+.
解答 解:根據圖知,右邊裝置中加入較稀的NaOH溶液,電解后得到較濃的NaOH溶液,說明b電極上發生的反應為2H2O-4e-=2H2↑+4OH-,所以b是陰極、a是陽極,左邊裝置中,加入稀硫酸和SO2,電解后得到較濃的硫酸,電極反應式為SO2+2H2O-2e-=SO42-+4H+;
A.通過以上分析知,b電極上得到的氣體是H2,即w是H2,故A錯誤;
B.b是陰極,連接電源負極,故B錯誤;
C.a電極上生成氫離子,需要硫酸根離子形成硫酸,所以離子交換膜c陰離子交換膜,故C錯誤;
D.左邊裝置中,加入稀硫酸和SO2,電解后得到較濃的硫酸,電極反應式為SO2+2H2O-2e-=SO42-+4H+,故D正確;
故選D.
點評 本題考查電解原理,為高頻考點,側重考查學生觀察、分析判斷、知識運用能力,明確各個電極上發生的反應、電極名稱的判斷是解本題關鍵,題目難度不大.


 亮點激活精編提優100分大試卷系列答案
亮點激活精編提優100分大試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | 若容器內壓強不再變化,則說明該反應己達平衡 | |
| B. | 反應前H2S物質的量為2.5mol | |
| C. | CO和H2S達平衡后的轉化率相同 | |
| D. | 若平衡后再加入CO,則正反應速率增大,逆反應速率減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 升高體系溫度,平衡常數K減小 | |
| B. | 增大體系壓強,平衡常數K不發生變化 | |
| C. | 平衡常數表達式為K=$\frac{[CO][{H}_{2}]}{[C][{H}_{2}O]}$ | |
| D. | 增加C(s)的量,平衡正向移動 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 溫度/℃ | 25 | 80 | 230 |
| 平衡常數 | 5×104 | 2 | 1.9×10-5 |
| A. | 上述生成Ni(CO)4的反應為放熱反應 | |
| B. | 在80℃時,測得某時刻Ni(CO)4、CO的濃度均為0.5 mol•L-1,則此時v正>v逆 | |
| C. | 25℃時反應Ni(CO)4(g) Ni(s)+4CO(g)的平衡常數為2×10-5 | |
| D. | 80℃達到平衡時,測得n(CO)=0.3 mol,則Ni(CO)4的平衡濃度為2 mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有②③ | B. | 只有③④ | C. | 只有①③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
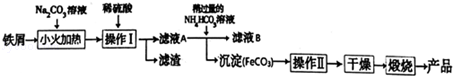
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氫氧燃料電池是一種將化學能轉化為電能的裝置 | |
| B. | 鐵船舶的外殼上鑲嵌鋅塊,可避免船體遭受腐蝕 | |
| C. | 鋼鐵腐蝕時負極的電極反應式:Fe-3e-═Fe+ | |
| D. | 工業上電解飽和食鹽水時陰極的電極反應式:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
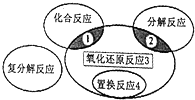 氧化還原反應與四種基本類型反應的關系如圖所示,則下列化學反應屬于區域3的是( )
氧化還原反應與四種基本類型反應的關系如圖所示,則下列化學反應屬于區域3的是( )| A. | 2H2+O2$\frac{\underline{\;點燃\;}}{\;}$2H2O | B. | 2Na2HCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O | ||
| C. | 2Na2O2+2H2O═4NaOH+O2↑ | D. | Zn+H2SO4═ZnSO4+H2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com