
| 物質 | NaCl | NaHCO3 | NH4Cl |
| 40℃時溶解度/g | 37 | 13 | 46 |
| 10℃時溶解度/g | 33 |
分析 (1)根據40℃時NaCl的溶解度,可以計算出434 g食鹽水中NaCl的質量和物質的量,計算44.8L(標準狀況)NH3的物質的量,反應式NH3+NaCl+CO2+H2O=NaHCO3↓+NH4Cl計算生成NaHCO3的質量和溶液中剩余的水的質量,再結合40℃時NaHCO3的溶解度計算可溶解NaHCO3的質量,析出NaHCO3的質量為生成的NaHCO3質量減去溶解的NaHCO3的質量;
(2)計算生成的NH4Cl質量和40℃時280.8 g水中可溶NH4Cl質量,比較二者的大小;
(3)根據10℃時NH4Cl的溶解度,計算280.8 g水中可溶NH4Cl質量,然后用生成的NH4Cl質量減去該部分質量即可;
(4)降溫至10℃時,NH4Cl溶液已飽和,可加入NaCl粉末,從而增加Cl-離子濃度,使NH4Cl的溶解平衡向左移動.
解答 解:根據40℃時NaCl的溶解度,可以計算出434 g食鹽水中NaCl的質量和物質的量:m(NaCl)=$\frac{37g}{137g}×434g$=117g,n(NaCl)=$\frac{117g}{58.5g/mol}$=2mol,
通入的NH3的物質的量:n(NH3)=$\frac{44.8L}{22.4L/mol}$=2mol,
由反應式NH3+NaCl+CO2+H2O=NaHCO3↓+NH4Cl可知各反應物和生成物之間物質的量相等的關系,
所以,可生成NaHCO3的質量:m(NaHCO3)=2 mol×84 g•mol-1=168 g,
溶液中剩余的水的質量為:m(H2O)=$\frac{434g×100g}{137g}$-2mol×18g/mol=280.8g,
這些水在40℃時可溶解NaHCO3的質量:m(NaHCO3)=$\frac{13g}{100g}×280.8g$=36.5g,
(1)析出NaHCO3的質量為:m(NaHCO3)=168 g-36.5 g=131.5 g,
答:可析出NaHCO3為131.5g;
(2)現有NH4Cl質量:m(NH4Cl)=2 mol×53.5 g•mol-1=107 g,40℃時,280.8 g水中可溶NH4Cl質量:$\frac{280.8g×46g}{100g}$=129.17g,因為129.17 g>107 g,所以NH4Cl不能析出,
答:NH4Cl不能析出;
(3)降溫至10℃,可析出NH4Cl:m(NH4Cl)=2 mol×53.5 g•mol-1-$\frac{280.8g×33g}{100g}$=14.3g,
答:若降溫至10℃,可析出NH4Cl14.3g;
(4)降溫至10℃時,NH4Cl溶液已飽和,可加入NaCl粉末,攪拌使之溶解,從而增加Cl-離子濃度,使NH4Cl的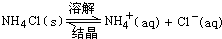 平衡向左移動,則可析出更多的NH4Cl晶體.
平衡向左移動,則可析出更多的NH4Cl晶體.
答:降溫至10℃時,若要析出更多的NH4Cl晶體,可加入NaCl粉末.
點評 本題考查了化學方程式的計算和沉淀溶解平衡的移動,難度中等,計算過程較為復雜、計算量較大,注意解答過程的簡潔和計算的準確性.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 800 | 1000 |
| 平衡常數K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向偏鋁酸鈉溶液中加入過量鹽酸:AlO2-+4H+=Al3++2H2O | |
| B. | MnO2與濃鹽酸混合加熱:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O | |
| C. | 等濃度等體積的Ba(OH)2溶液和NaHSO4溶液混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| D. | 用NaOH溶液吸收少量H2S氣體:OH-+H2S=HS-+H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 只有① | B. | ①或② | C. | 只有④ | D. | ③或④ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 錫中加入一定量的鉛制成焊錫,目的使被焊接的部分更牢固,更不易被氧化 | |
| B. | 聚乙烯制成塑料薄膜,用于食品、藥品包裝的材料 | |
| C. | 大量燃燒化石燃料是造成霧霾天氣的一種重要因素 | |
| D. | 含重金屬離子的電鍍廢液不能隨意排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 用有機溶劑從青蒿中提取青蒿素,主要采用萃取的方法 | |
| B. | 青蒿素的分子式為C15H22O5 | |
| C. | 青蒿素通過還原反應可制得雙氫青蒿素 | |
| D. | 青蒿素和雙氫青蒿素都是芳香族化合物 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大 | B. | 減小 | C. | 不變 | D. | 不能確定 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com