
分析 濃鹽酸和二氧化錳在加熱條件下生成氯氣,但稀鹽酸和二氧化錳在加熱條件下不反應,據此分析解答.
解答 解:濃鹽酸和二氧化錳在加熱條件下生成氯氣,但稀鹽酸和二氧化錳在加熱條件下不反應,所以①中濃鹽酸在反應中濃度達到一定程度時就不和二氧化錳反應了,導致生成的氯氣物質的量小于1mol,②中濃鹽酸足量,當二氧化錳完全反應時生成1mol氯氣,所以二者產生的氯氣不一樣多,
答:二者產生的氯氣不一樣多;因為濃鹽酸和二氧化錳反應生成氯氣而稀鹽酸和二氧化錳不反應,當①中濃鹽酸在反應中濃度達到一定程度時就不和二氧化錳反應了,②中濃鹽酸足量,所以前者生成的氯氣小于后者.
點評 本題考查化學方程式的有關計算,為高頻考點,側重考查學生分析判斷能力,明確濃鹽酸、稀鹽酸性質差異性是解本題關鍵,注意反應①中鹽酸濃度的變化,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{15}^{52}$P的原子核中含有15個中子 | |
| B. | ${\;}_{15}^{52}$P的相對原子質量為32 | |
| C. | ${\;}_{15}^{52}$P原子的質量數是17 | |
| D. | ${\;}_{15}^{52}$P原子中含有的電子數和質子數都是15 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
| 元素 | 相關信息 |
| X | X的基態原子L層電子數是K層電子數的2倍 |
| Y | Y是地殼中含量最高的元素 |
| Z | Z的基態原子最外層電子排布式為3s23p1 |
| W | W有多種化合價,其白色氫氧化物在空氣中會迅速變成灰綠色,最后變成紅褐色 |
 ;
;查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| H2(g) | Br2(g) | HBr(g) |
| 436kJ | akJ | 369kJ |
| A. | 200 | B. | 230 | C. | 260 | D. | 404 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
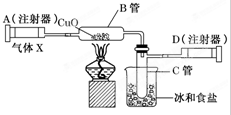 如圖所示的實驗裝置可用來測定含兩種元素的氣體X的分子式.
如圖所示的實驗裝置可用來測定含兩種元素的氣體X的分子式.查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
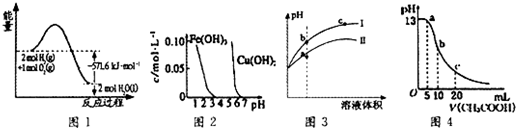
| A. | 圖1表示H2與O2發生反應過程中的能量變化,H2的燃燒熱為285.8 kJ/mol | |
| B. | 由圖2得出若除去CuSO4溶液中的Fe3+,可采用向溶液中加入適量CuO,調節溶液的pH至4左右 | |
| C. | 圖3表示用水稀釋pH相同的鹽酸和醋酸時溶液的pH變化曲線,其中Ⅰ表示醋酸,Ⅱ表示鹽酸,且溶液導電性:c>b>a | |
| D. | 圖4表示常溫下向體積為10 mL0.1 mol/LNaOH溶液中逐滴加入0.1 mol/LCH3COOH溶液后溶液的pH變化曲線,則b點處有:c(CH3COOH)+c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=7的NaHSO3與Na2SO3混合溶液中:3c(Na+)=c(HSO3-)+c(SO32-) | |
| B. | 0.1mol•L-1的KHA溶液,其PH=10:c(K+)>c(OH-)>c(HA-)>c(H+) | |
| C. | 20mL0.1mol•L-1醋酸鈉溶液與10mL 0.1mol•L-1鹽酸混合后的溶液中: 2 c(H+)+c(CH3COOH)=c(CH3COO-)+2 c(OH-) | |
| D. | 在25mL 0.1 mol•L-1NaOH溶液中逐滴加入0.2mol•L-1CH3COOH溶液,溶液pH變化如圖所示,在A、B間任一點,溶液中一定都存在下列關系:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)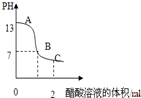 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com