
| 元素 | T | X | Y | Z |
| 性質結構信息 | 原子核外s電子總數等于p電子總數;人體內含量最多的元素,且其單質是常見的助燃劑 | 單質為雙原子分子,分子中含有3對共用電子對,常溫下單質性質穩定,但其原子較活潑 | 第3周期元素的簡單離子中半徑最小 | 第4周期元素,M電子層為全充滿狀態,最外層只有一個電子的原子 |
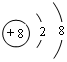 ;寫出元素X的氣態氫化物的電子式
;寫出元素X的氣態氫化物的電子式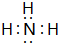 ;X形成的單質分子,含1個σ鍵,2個π鍵.寫出Z元素原子的外圍電子排布式3d104s1;元素Y的原子核外共有2種形狀不同的電子云.
;X形成的單質分子,含1個σ鍵,2個π鍵.寫出Z元素原子的外圍電子排布式3d104s1;元素Y的原子核外共有2種形狀不同的電子云.分析 T原子核外s電子總數等于p電子總數;人體內含量最多的元素,且其單質是常見的助燃劑,應為O元素,X單質為雙原子分子,分子中含有3對共用電子對,常溫下單質性質穩定,但其原子較活潑,為N元素,Y第3周期元素的簡單離子中半徑最小,應為Al,Z第4周期元素,M電子層為全充滿狀態,最外層只有一個電子的原子,應為Cu,結合對應單質、化合物的性質以及題目要求解答該題.
解答 解:(1)元素T的離子為O2-,O2-離子結構示意圖為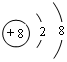 ,元素X的氣態氫化物為NH3,電子式為
,元素X的氣態氫化物為NH3,電子式為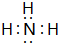 ,N2分子中存在N≡N,含有1個σ鍵、2個π鍵,Z為Cu,外圍電子排布式為3d104s1,Y為Al,核外有s、p能級,則有2種不同形狀的電子云,
,N2分子中存在N≡N,含有1個σ鍵、2個π鍵,Z為Cu,外圍電子排布式為3d104s1,Y為Al,核外有s、p能級,則有2種不同形狀的電子云,
故答案為: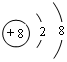 ;
;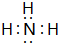 ;1;2;3d104s1;2;
;1;2;3d104s1;2;
(2)Z單質為Al,Y最高價氧化物的水化物為NaOH,二者反應生成偏鋁酸鈉與氫氣,反應的離子方程式為:2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案為:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)元素氧與氟元素相比,非金屬性較強的是F元素,
a.單質顏色屬于物理性質,不能比較元素非金屬性強弱,故a錯誤;
b.氟氣與T的氫化物劇烈反應,產生T的單質,說明氟氣氧化性更強,可以說明氟元素非金屬性強,故b正確;
c.氟與T形成的化合物中T元素呈正價態,說明F元素對鍵合電子吸引更強,則氟元素非金屬性更強,故c正確;
d.非金屬性強弱與獲得電子難易程度有關,與獲得電子數目多少無關,故d錯誤.
故答案為:F;bc.
點評 本題考查結構性質位置關系應用,為高考常見題型,側重對化學用語與元素周期律的考查,注意掌握金屬性、非金屬性強弱比較,難度不大.


科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,11.2LH2O 含有的分子數為0.5NA | |
| B. | 在常溫常壓下,11.2LCl2含有的分子數為0.5NA | |
| C. | 含有NA個氬原子的氬氣在標準狀況下的體積約為11.2L | |
| D. | 25℃,1.01×105 Pa,64gSO2中含有的原子數為3NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Fe分別與氯氣和稀鹽酸反應所得氯化物相同 | |
| B. | K、Zn分別與不足量的稀硫酸反應所得溶液均呈中性 | |
| C. | Li、Na、K的原子半徑和密度隨原子序數的增加而增大 | |
| D. | C、S、Cl的最高價氧化物對應水化物的酸性逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 分子中處于四面體中心位置的碳原子數為a,一定在同一直線上的碳原子個數為b,一定在同一平面上的碳原子數為c.則a、b、c分別為( )
分子中處于四面體中心位置的碳原子數為a,一定在同一直線上的碳原子個數為b,一定在同一平面上的碳原子數為c.則a、b、c分別為( )| A. | 4、4、7 | B. | 4、3、6 | C. | 3、5、4 | D. | 2、6、4 |
查看答案和解析>>
科目:高中化學 來源: 題型:計算題
查看答案和解析>>
科目:高中化學 來源:2016-2017學年河北省高一上10月月考化學試卷(解析版) 題型:選擇題
關于KOH溶液和Fe(OH)3膠體描述正確的是
A.兩者的分散質都屬于堿
B.兩者均為有色不透明的分散系
C.兩者分散質的直徑都介于10-9 ~10-7m之間
D.一束光線分別通過時,兩者都會出現明顯的光帶
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com