
| A. | 標準狀況下,2.24LNO2分子總數小于0.1NA | |
| B. | 50ml,18.4 mol/L濃硫酸與足量銅微熱反應,生成SO2分子的數目為0.46NA | |
| C. | 標準狀況下,33.6 L氟化氫中含有氟原子的數目為1.5NA | |
| D. | 6.8g液態KHSO4中含有0.1NA個陽離子 |
分析 A.二氧化氮與四氧化二氮之間存在轉化平衡;
B.稀硫酸與銅不發生反應,則銅足量時反應生成的二氧化硫的量減小;
C.標準狀況下,氟化氫的狀態不是氣體;
D.液態硫酸氫鉀中含有的陽離子只有鉀離子.
解答 解:A.標準狀況下22.4L二氧化氮的物質的量為1mol,由于部分二氧化氮轉化成四氧化二氮,則含有二氧化氮的物質的量小于1mol,含有NO2分子總數小于0.1NA,故A正確;
B.50mL 18.4 mol/L濃硫酸中含有硫酸的物質的量為:18.4mol/L×0.05L=0.92mol,銅與濃硫酸的反應中,消耗0.92mol硫酸會生成0.46mol二氧化硫,由于濃硫酸變成稀硫酸后反應停止,則銅足量時反應生成的二氧化硫小于0.46mol,生成SO2分子的數目小于0.46NA,故B錯誤;
C.標準狀況下,HF不是氣體,不能使用標準狀況下的氣體摩爾體積計算33.6L氟化氫的物質的量,故C錯誤;
D.6.8g硫酸氫鉀的物質的量為:$\frac{6.8g}{136g/mol}$=0.05mol,0.05mol液態硫酸氫鉀中含有0.05mol鉀離子和0.05mol硫酸氫根離子,則含有陽離子的數目小于0.1NA,故D錯誤;
故選A.
點評 本題考查了阿伏伽德羅常數的綜合應用,題目難度不大,明確物質的量與阿伏伽德羅常數、摩爾質量、氣體摩爾體積等之間的關系為解答關鍵,C為易錯點,注意標準狀況下HF不是氣體.


科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:Na<Cl | B. | 熱穩定性:HCI<HF | ||
| C. | 離子半徑:F-<Mg2+ | D. | 堿性:NaOH<Mg(OH)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
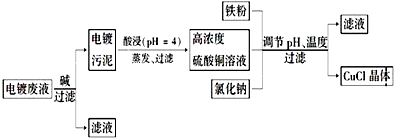
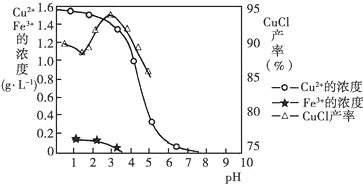
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H+、Na+、NO3-、CO32- | B. | H+、Na+、ClO-、Cl- | ||
| C. | K+、HCO3-、Cl-、OH- | D. | Na+、Mg2+、NO3-、SO42- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 利用外接直流電源保護鐵質建筑物,屬于電化學中犧牲陽極的陰極保護法 | |
| B. | 科學儀器的使用利于我們認識物質的微觀世界,現在人們借助掃描隧道顯微鏡,應用SMT技術可以“看”到越來越細微的結構,并實現對原子或分子的操縱 | |
| C. | 人們通常用標準燃燒熱或熱值來衡量燃料燃燒放出熱量的大小,某物質的熱值越高則其標準燃燒熱越大 | |
| D. | 汽車尾氣催化轉化裝置可將尾氣中的NO和CO等有害氣體轉化為N2和CO2,該裝置中的催化劑可降低NO和CO反應的活化能,加快該反應的速率,同時能提高該反應的平衡轉化率 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 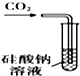 甲裝置:可用來證明碳酸的酸性比硅酸強 | |
| B. | 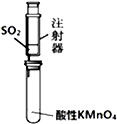 乙裝置:可用來檢驗二氧化硫氣體 | |
| C. | 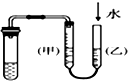 丙裝置:用圖示的方法不能檢查此裝置的氣密性 | |
| D. |  丁裝置:先從①口進氣集滿二氧化碳,再從②口進氣,可收集氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | ① | B. | ② | C. | ③ | D. | ④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
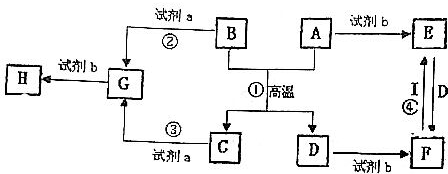
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁粉在氧氣中燃燒生成Al2O3,故鐵絲在氧氣中燃燒生成Fe2O3 | |
| B. | 鐵能從硫酸銅溶液中置換出銅,故鈉也能從硫酸銅溶液中置換出銅 | |
| C. | 鈉與氧氣、水等反應時鈉均作還原劑,故金屬單質參與化學反應時金屬均作還原劑 | |
| D. | 活潑金屬鈉保存在煤油中,故活潑金屬鋁也保存在煤油中 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com