
分析 (1)等物質的量時,獲得電子越多,消毒效率越高;
(2)NH2Cl與水反應生成的HClO和NH3,HClO有強氧化性,具備殺菌作用.
解答 解:(1)物質的量都為1mol時,Cl2獲得2mol電子,H2O2獲得2mol電子,ClO2獲得5mol電子,O3獲得2mol電子,ClO2得到的電子最多,消毒效率最高,
故答案為:C;
(2)NH2Cl與水反應生成的HClO和NH3,反應方程式為NH2Cl+H2O=NH3+HClO,HClO有強氧化性,具備殺菌作用,
故答案為:NH2Cl+H2O=NH3+HClO.
點評 本題考查氧化還原反應,為高頻考點,側重于學生的分析能力的考查,難度中等,(2)為易錯點,注意結合氯氨(NH2Cl)可作為殺菌劑,確定發生水解反應有HClO生成.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 、加入氯化鐵的目的是加深溶液顏色,放大實驗現象 | |
| B. | 、本實驗的目的是研究濃度對雙氧水分解速率的影響 | |
| C. | 、本實驗過程中A、B試管都不明顯,可以將那個很不明顯的試管放入熱水浴中來觀察 | |
| D. | 、小明剛把A藥品準備好,就有事情出去了,第二天繼續這個實驗來進行比較 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將pH=10的濃氨水稀釋,溶液中所有離子的濃度都減小 | |
| B. | CaCO3(s)=CaO(s)+CO2(g)室溫下不能自發進行,說明該反應的△H<0 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他條件不變時升高溫度,反應速率V(H2)和氫氣的平衡轉化率均增大 | |
| D. | pH=3的鹽酸和pH=11的氨水等體積混合液中,c(H+)<c(OH-) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
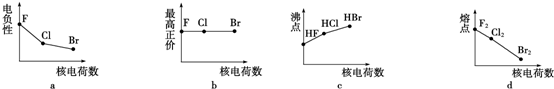
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1.00molNaCl中含有6.02×1023個NaCl分子 | |
| B. | 從100mL,1 mol/L的NaCl溶液中取出10 mL,其物質的量濃度是0.1 mol/L | |
| C. | 1.00mol NaCl中,所有Na+的最外層電子總數為8×6.02×1023 | |
| D. | 欲配制1.00L,1.00mol•L-1的NaCl溶液,可將58.5g NaCl溶于1.00L水中 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 洗凈的錐形瓶和容量瓶可以放進烘箱中烘干 | |
| B. | 酸式滴定管裝標準溶液前,必須先用該溶液潤洗 | |
| C. | 酸堿滴定實驗中,用待滴定溶液潤洗錐形瓶以減小實驗誤差 | |
| D. | 所有玻璃儀器加熱時均需墊石棉網 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 春蠶到死絲方盡,蠟炬成灰淚始干 | B. | 粉身碎骨渾不怕,要留清白在人間 | ||
| C. | 爆竹聲中一歲除,春風送暖入屠蘇 | D. | 野火燒不盡,春風吹又生 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氧化鋁熔點高,可用于制作耐火材料 | |
| B. | 氫氧化鋁難溶于水,可用于制胃酸中和劑 | |
| C. | Na2O2具有強氧化性,可用作自來水的消毒劑 | |
| D. | 氧化鐵能與酸反應,可用于制作紅色涂料 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com