
 如圖是在航天用高壓氫鎳電池基礎上發展起來的一種金屬氫化物鎳電池(MH-Ni電池).下列有關說法不正確的是( )
如圖是在航天用高壓氫鎳電池基礎上發展起來的一種金屬氫化物鎳電池(MH-Ni電池).下列有關說法不正確的是( )| A. | 放電時正極反應為:NiOOH+H2O+e-=Ni(OH)2+OH- | |
| B. | 電池的電解液可為KOH溶液 | |
| C. | 充電時負極反應為:MH+OH-=M+H2O+e- | |
| D. | MH是一類儲氫材料,其氫密度越大,電池的能量密度越高 |
分析 鎳氫電池中主要為KOH作電解液充電時,陽極反應:Ni(OH)2+OH-=NiOOH+H2O+e-陰極反應:M+H2O+e-=MH+OH-,總反應:M+Ni(OH)2=MH+NiOOH;
放電時,正極:NiOOH+H2O+e-=Ni(OH)2+OH-,負極:MH+OH--e-=M+H2O,總反應:MH+NiOOH=M+Ni(OH)2 ,以上式中M為儲氫合金,MH為吸附了氫原子的儲氫合金.
解答 解:A、放電時,正極:NiOOH+H2O+e-=Ni(OH)2+OH-,故A正確;
B、為了防止MH被氫離子氧化,鎳氫電池中電解液為堿性溶液,主要為KOH作電解液,故B正確;
C、充電時,負極作陰極,陰極反應為M+H2O+e-=MH+OH-,故C錯誤;
D、M為儲氫合金,MH為吸附了氫原子的儲氫合金,儲氫材料,其氫密度越大,電池的能量密度越高,故D正確;
故選C.
點評 本題考查了原電池和電解池原理,明確題給信息的含義是解本題關鍵,難點的電極反應式的書寫,題目難度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 石油、天然氣等燃燒產生大量二氧化碳 | |
| B. | 大量燃燒含硫量高的煤產生二氧化硫 | |
| C. | 森林遭到亂砍爛伐,破壞了生態環境 | |
| D. | 各種機動車排放的尾氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol H2SO4 的質量為98 g•mol-1 | |
| B. | H2SO4的摩爾質量為98 g | |
| C. | 9.8 g H2SO4含有NA個H2SO4分子 | |
| D. | 6.02×1022個H2SO4分子的質量為9.8 g |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
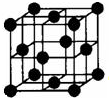 早期發現的一種天然二十面體準晶顆粒由Al、Cu、Fe三種金屬元素組成.回答下列問題:
早期發現的一種天然二十面體準晶顆粒由Al、Cu、Fe三種金屬元素組成.回答下列問題:查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 在外電路中,電子由銀電極流向銅電極 | |
| B. | 取出鹽橋后,電流計的指針仍發生偏轉 | |
| C. | 外電路中每通過0.1 mol電子,銅的質量理論上減小6.4 g | |
| D. | 原電池的總反應式為Cu+2AgNO3=2Ag+Cu(NO3)2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
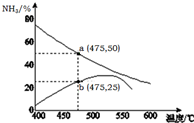 氨是一種重要的化工原料,也是重要的工業產品,在工農業生產和國防等領域發揮著重要作用.
氨是一種重要的化工原料,也是重要的工業產品,在工農業生產和國防等領域發揮著重要作用.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
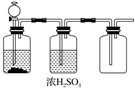
| A. | FeS和稀H2SO4 | B. | 加熱NaCl和濃H2SO4制HCl | ||
| C. | 大理石和稀鹽酸 | D. | MnO2和濃鹽酸 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com