

分析 (1)根據儀器特征,可知儀器C是干燥管;F裝置應是Cl2和KI反應,還需要連接尾氣處理裝置,所以應長管進氣,短管出氣;
(2)在2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O反應中,NaClO3中氯元素化合價由+5價降低為+4價,NaClO3是氧化劑,還原產物是ClO2;HCl中氯元素化合價由-1價升高為0價,HCl是還原劑,氧化產物是Cl2,根據產物可知起還原劑與酸性的氯化氫各占一半;為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢;
(3)氯氣有毒,能夠與碘化鉀反應,被碘化鉀溶液吸收;
(4)在酸性條件下NaClO2可發生反應生成NaCl并釋放出ClO2,根據元素守恒可知應還有水生成,據此分析書寫離子方程式; 在ClO2釋放實驗中,打開E的活塞,D中發生反應,則裝置F的作用是驗證是否有ClO2 生成;
(5)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度.
解答 解:(1)儀器C具有球形特征,據此可知該儀器是干燥管;F裝置應是Cl2和KI反應,還需要連接尾氣處理裝置,所以應長管進氣,短管出氣,故選b,
故答案為:干燥管;b;
(2)在氧化還原反應中,反應物中元素化合價降低的物質為氧化劑,化合價升高的物質為還原劑,2NaClO3+4HCl=2ClO2↑+Cl2↑+2NaCl+2H2O反應中,NaClO3中氯元素化合價由+5價降低為+4價,NaClO3是氧化劑,還原產物是ClO2;HCl中氯元素化合價由-1價升高為0價,HCl是還原劑,氧化產物是Cl2,根據氧化產物是Cl2,可知起還原劑與酸性的氯化氫各占一半,所以該反應中氧化劑與還原劑物質的量之比為1:1,為使ClO2在D中被穩定劑充分吸收,產生ClO2的速率要慢,
故答案為:1:1;慢;
(3)氯氣有毒,能夠與碘化鉀反應,被碘化鉀溶液吸收,所以F的作用為吸收Cl2,
故答案為:吸收Cl2;
(4)在酸性條件下NaClO2可發生反應生成NaCl并釋放出ClO2,根據元素守恒可知應還有水生成,該反應的離子方程式為:4H++5ClO2-=Cl-+4ClO2↑+2H2O; 在ClO2釋放實驗中,打開E的活塞,D中發生反應,則裝置F的作用是驗證是否有ClO2 生成,
故答案為:4H++5ClO2-=Cl-+4ClO2↑+2H2O;驗證是否有ClO2 生成;
(5)由圖可知,穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度,所以穩定劑Ⅱ好,
故答案為:穩定劑Ⅱ;穩定劑Ⅱ可以緩慢釋放ClO2,能較長時間維持保鮮所需的濃度.
點評 本題以ClO2的制備、吸收、釋放為載體,考查實驗制備方案設計、基本操作、對裝置及操作的分析評價等,注意根據問題進行制備流程分析,題目難度中等.


科目:高中化學 來源: 題型:選擇題
| A. | 離子化合物可能含共價鍵 | B. | 共價化合物可能含離子鍵 | ||
| C. | 離子化合物中只含離子鍵 | D. | 離子化合物一定不含共價鍵 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
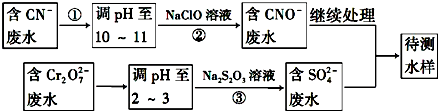
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH3OH的燃燒熱(△H)為-192.9kJ•mol-1 | |
| B. | 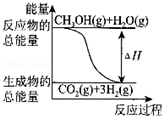 反應①中的能量變化如圖所示 | |
| C. | CH3OH轉變成H2的過程一定要吸收能量 | |
| D. | 根據②推知反應:CH3OH(l)+O2(g)═CO2(g)+2H2(g)的△H>-192.9kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 4.6gNO2與N2O4的混合氣體中所含氮原子數為0.1NA | |
| B. | 常溫常壓下1.6g甲烷所含共用電子對數為0.1NA | |
| C. | 標準狀況下,6.72LCO2與足量Na2O2反應轉移電子數為0.6NA | |
| D. | 50ml 98%濃硫酸(密度為1.84g•cm-3)與足量銅共熱,轉移的電子數為0.92NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 如圖是在航天用高壓氫鎳電池基礎上發展起來的一種金屬氫化物鎳電池(MH-Ni電池).下列有關說法不正確的是( )
如圖是在航天用高壓氫鎳電池基礎上發展起來的一種金屬氫化物鎳電池(MH-Ni電池).下列有關說法不正確的是( )| A. | 放電時正極反應為:NiOOH+H2O+e-=Ni(OH)2+OH- | |
| B. | 電池的電解液可為KOH溶液 | |
| C. | 充電時負極反應為:MH+OH-=M+H2O+e- | |
| D. | MH是一類儲氫材料,其氫密度越大,電池的能量密度越高 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 生成 SO3 為 2 mol | |
| B. | SO2 和 SO3 物質的量之和一定為 3 mol | |
| C. | 1molO2 恰好反應完 | |
| D. | SO2 的物質的量和 SO3 物質的量一定相等 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯氣溶于水中:Cl2+H2O=2H++Cl-+ClO- | |
| B. | 硫酸氫鈉溶液與氫氧化鋇溶液混合至混合液呈中性:2HSO4-+Ba2++2OH-=BaSO4↓+2H2O+SO42- | |
| C. | 向雙氧水中加入稀硫酸和KI溶液:H2O2+2H++2I-=I2+2H2O | |
| D. | 用銅作陽極電解CuSO4溶液:2Cu2++2H2O$\frac{\underline{\;電解\;}}{\;}$2Cu+O2↑+4H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
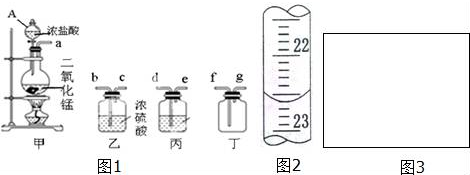
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com