
某學習小組探究溴乙烷的消去反應并驗證產物。

實驗過程:組裝如圖1所示裝置,檢查裝置氣密性,向燒瓶中注入10mL溴乙烷和15mL飽和氫氧化鈉乙醇溶液,微熱,觀察實驗現象。一段時間后,觀察到酸性KMnO4溶液顏色褪去。
(1)請寫出溴乙烷的消去反應的化學方程式:
(2)甲同學認為酸性KMnO4溶液顏色褪去說明溴乙烷發生了消去反應,生成了乙烯;而乙同學卻認為甲同學的說法不嚴謹,請說明原因: 。
(3)丙同學認為只要對實驗裝置進行適當改進,即可避免對乙烯氣體檢驗的干擾,改進方法: 。
改進實驗裝置后,再次進行實驗,卻又發現小試管中溶液顏色褪色不明顯。該小組再次查閱資料,對實驗進行進一步的改進。
資料一:溴乙烷于55℃時,在飽和氫氧化鈉的乙醇溶液中發生取代反應的產物的百分比為99%,而消去反應產物僅為1%。
資料二:溴乙烷發生消去反應比較適宜的反應溫度為90℃~110℃,在該范圍,溫度越高,產生乙烯的速率越快。
資料三:溴乙烷的沸點:38.2℃。
(4)結合資料一、二可知,丙同學改進實驗裝置后,溶液顏色褪色不明顯的原因可能是 ,此時發生反應的化學方程式為 。
(5)結合資料二、三,你認為還應該在實驗裝置中增加的兩種儀器是
① ②
科目:高中化學 來源:2015-2016學年遼寧省協作校高二下期末化學試卷(解析版) 題型:選擇題
向2.2克某飽和一元醛中加入足量銀氨溶液,在一定條件下充分反應后析出10.8克銀,該醛是( )
A.CH3CH2CH2CHO B.CH3CHO C.CH3CH2CHO D.CH3CH(CH3)CHO
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省泰安市高一下學期期末考試化學試卷(解析版) 題型:計算題
取標準狀況下CH4和過量O2的混合氣體840 mL,點燃,將燃燒后的氣體用過量堿石灰吸收,堿石灰增重0.600g。請計算:
(1)堿石灰吸收后所剩氣體的體積(標準狀況下);
(2)原混合氣體中CH4與O2的體積比。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省泰安市高一下學期期末考試化學試卷(解析版) 題型:選擇題
某短周期非金屬元素的原子核外最外層電子數是次外層電子數的一半,該元素( )
A. 在自然界中以化合態的形式存在
B. 單質常用作半導體材料和光導纖維
C. 最高價氧化物不與酸反應
D. 氣態氫化物比甲烷穩定
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山東省泰安市高一下學期期末考試化學試卷(解析版) 題型:選擇題
下圖表示某有機反應,該反應的類型為( )
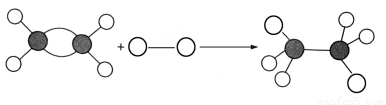
A.加成反應 B.取代反應
C.氧化反應 D.化合反應
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高二下期末化學試卷(解析版) 題型:選擇題
下列各組混合物無論以何種比例混合,只要總的物質的量一定,完全燃燒時消耗氧氣的量是定值的是( )
A. CH2O、C2H4O2、C6H12O6
B. H2、CO、CH3OH
C. CH2=CH2、C2H5OH、HOCH2CH2COOH
D. C6H6、C5H12、C7H6O2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年甘肅省高二下期末化學試卷(解析版) 題型:選擇題
某一氯代烴A經水解后再氧化,最終得到有機物B,A的一種同分異構體經水解得到有機物C,B和C可發生酯化反應生成酯D,則D可能是( )
A.(CH3)2CHCOOC(CH3)3
B.(CH3)2CHCOOCH2CH(CH3)2
C.CH3(CH2)2COOCH2(CH2)2CH3
D.(CH3)2CHCOOCH2CH2CH3
查看答案和解析>>
科目:高中化學 來源:2015-2016學年重慶一中高一下期末化學試卷(解析版) 題型:填空題
2SO2(g)+O2(g) 2SO3(g) ΔH<0,是工業制硫酸的主要反應之一。
2SO3(g) ΔH<0,是工業制硫酸的主要反應之一。
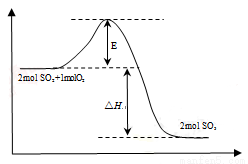
(1)該反應過程的能量變化如右圖所示:E的大小對該反應的反應熱有無影響_______(填“有”或“無”),該反應通常用V2O5作催化劑,加入V2O5后,改變的是圖中的_______。
A.△H B.E C.△H – E D.△H + E
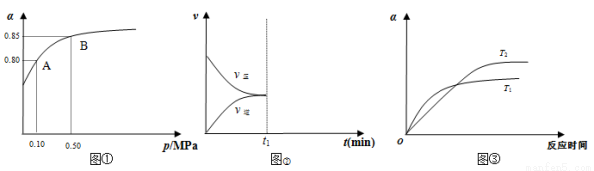
(2)某溫度下,甲同學將2 mol SO2和1 mol O2置于密閉容器中,反應達平衡后,SO2的平衡轉化率(α)與體系總壓強(p)的關系如圖①所示,若A點二氧化硫的平衡濃度為0.04 mol/L,則容器的體積為_______L;圖①中B點SO2、O2、SO3的平衡濃度之比為________________;反應到達平衡時,時間t1時縮小容器體積,請在圖②中畫出時間t1之后反應速率變化圖像;圖③為壓強等于0.50 MPa時不同溫度下SO2轉化率與溫度關系圖,圖中T2_____T1(填寫“大于”或“小于”)
(3)在2 L的密閉容器中,乙同學投入2 mol SO2和b mol O2,25 min時達到平衡,如下圖所示,在35 min時,改變某一條件,經過一段時間后,70 min時,反應再次達到平衡,回答下列問題:

①10 min時,v(SO2)正________v(SO3)逆(填“>”“<”或“=”)
②求0~10 min時,v(O2)=______________
③反應開始至35 min時,測得反應共放熱138.6 kJ,則反應2SO2(g)+O2(g) 2SO3(g)△H=____kJ/mol
2SO3(g)△H=____kJ/mol
④35 min時,改變的條件可能是___________________
a.加入更多的V2O5
b.從容器中分離出少量O2
c.投入一定量的SO3
d.降低反應溫度
e.往容器中加入N2,使容器壓強增大
查看答案和解析>>
科目:高中化學 來源:2015-2016學年青海省高一下期末化學試卷(解析版) 題型:選擇題
下列遞變情況中,正確的是 ( )
A. Na、Mg、Al原子的最外層電子數依次減少
B. Si、P、S元素的最高正價依次降低
C. C、N、O的原子半徑依次減小
D. Li、Na、K的金屬性依次減弱
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com