

| A. | ①圖象中如果縱坐標為正反應速率,則t時刻改變的條件可以為升溫或加壓 | |
| B. | ②圖象中縱坐標可以為鎵的轉化率 | |
| C. | ③圖象中縱坐標可以為化學反應速率 | |
| D. | ④圖象中縱坐標可以為體系內混合氣體平均相對分子質量 |
分析 A、①圖象中如果縱坐標為正反應速率,升高溫度或增大壓強,反應速率增大;
B、改變壓強對Ga是固體無影響;
C、Ga是固體,其質量不影響反應速率;
D、相同壓強下,升高溫度,平衡逆向移動,平均相對分子質量增大;相同溫度下,增大壓強,平衡逆向移動,平均相對分子質量增大.
解答 解:A、①圖象中如果縱坐標為正反應速率,升高溫度或增大壓強,反應速率增大,圖象符合題意,故A正確;
B、Ga是固體,沒有濃度可言,壓強改變對固體物影響,故B錯誤;
C、Ga是固體,其質量不影響反應速率,故C錯誤;
D、相同壓強下,升高溫度,平衡逆向移動,平均相對分子質量增大;相同溫度下,增大壓強,平衡逆向移動,平均相對分子質量增大,所以溫度高的曲線在上面,故D錯誤;
故選A.
點評 本題考查了化學平衡的建立過程、化學平衡影響因素分析,圖象中曲線變化和化學平衡移動原理的綜合應用,注意平衡移動方向和影響因素的理解,題目難度中等.


 怎樣學好牛津英語系列答案
怎樣學好牛津英語系列答案 導學教程高中新課標系列答案
導學教程高中新課標系列答案科目:高中化學 來源: 題型:解答題
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 第2周期 | ⑥ | ⑦ | ||||||
| 第3周期 | ① | ③ | ⑤ | ⑩ | ⑧ | |||
| 第4周期 | ② | ④ | ⑨ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
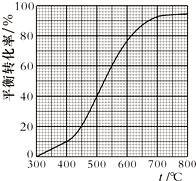 工業上以乙苯催化脫氫制取苯乙烯的反應如下:
工業上以乙苯催化脫氫制取苯乙烯的反應如下: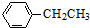 (g)$\stackrel{催化劑}{?}$
(g)$\stackrel{催化劑}{?}$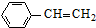 (g)+H2(g)
(g)+H2(g)| A. | 400℃時,向體系中通入水蒸氣,v(正)、v(逆) 均減小,且乙苯轉化率降低 | |
| B. | 500℃時,向體系中通入乙苯、苯乙烯、氫氣各0.1x mol,平衡不移動 | |
| C. | 550℃時,用平衡分壓代替平衡濃度表示的化學平衡常數Kp=$\frac{9}{16}$×p總 | |
| D. | 550℃時平衡體系中苯乙烯的體積分數是450℃時的3倍 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,在pH=7的醋酸鈉和醋酸混合溶液中,c(CH3COO-)>c(Na+) | |
| B. | 稀釋醋酸溶液,溶液中所有離子的濃度均降低 | |
| C. | 在pH=5的氯化鈉和稀硝酸的混合溶液中,c(Na+)=c(Cl-) | |
| D. | 在0.1 mol•L-1的硫化鈉溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
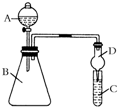 某同學為驗證元素周期表中元素性質的遞變規律,利用如圖裝置可驗證同主族非金屬性的變化規律.設計了如下系列實驗.
某同學為驗證元素周期表中元素性質的遞變規律,利用如圖裝置可驗證同主族非金屬性的變化規律.設計了如下系列實驗.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com