
分析 (1)存在的分子有H2O、H2A,則H2A為弱酸;
(2)等體積混合生成Na2A,水解顯堿性,離子水解以第一步為主;由反應式Ba2++A2-=BaA↓可得:沉淀后A2-過量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根據BaA的Ksp可得c(Ba2+);
(3)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,顯酸性,則酸過量,以此分析.
解答 解:(1)存在的分子有H2O、H2A,則H2A為弱酸,電離方程式為H2A?H++HA-、HA-?H++A2-,故答案為:H2A?H++HA-、HA-?H++A2-;
(2)等體積混合生成Na2A,水解顯堿性,pH>7,離子水解以第一步為主,則離子濃度關系為c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+),由反應式Ba2++A2-=BaA↓可得:沉淀后A2-過量0.01mol,溶液中c(A2-)=$\frac{0.01mol}{30×1{0}^{-3}L}$=$\frac{1}{3}$mol•L-1,根據BaA的Ksp=c(Ba2+)•c(A2-)可得c(Ba2+)=$\frac{{K}_{sp}}{c({A}^{2-})}$=$\frac{\frac{1.8×1{0}^{-10}}{1}}{3}$
=5.4×10-10 mol•L-1;
故答案為:>;c(Na+)>c(A2-)>c(OH-)>c(HA-)>c(H+);5.4×10-10;
(3)混合溶液c(H+)/c(OH-)=104,c(H+)=10-5mol/L,顯酸性,則酸過量,H2A為弱酸,pH=3的H2A溶液與pH=11的NaOH溶液混合時酸的濃度大于堿的濃度,則二者體積關系不確定,大于、小于或等于都可能酸過量,故答案為:均有可能.
點評 本題考查較綜合,涉及酸堿混合的定性分析、pH、電離與水解、電離方程式等,把握溶液中的溶質及電離與水解的趨勢、相互影響即可解答,題目難度中等.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 硒化氫比硫化氫穩定 | |
| B. | 原子序數為 34 | |
| C. | 最高價氧化物的水化物的分子式為:H2SeO4 | |
| D. | Se 的非金屬性比 Br 弱 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
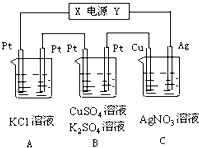 如圖所示,若電解5min時銅電極的質量增加2.16g,B中一根Pt電極質量增加0.32g,且此時B中兩極都有氣體產生.試回答:
如圖所示,若電解5min時銅電極的質量增加2.16g,B中一根Pt電極質量增加0.32g,且此時B中兩極都有氣體產生.試回答:查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 干冰和碘分別變為氣體 | B. | 干冰和氯化銨分別受熱變為氣體 | ||
| C. | 二氧化硅和鐵分別受熱熔化 | D. | 食鹽和葡萄糖分別溶解在水中 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③⑤ | B. | ①②③④⑤ | C. | ①②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
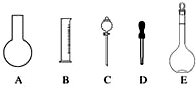 實驗室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題:
實驗室需要0.1mol•L-1 NaOH溶液450mL和0.5mol•L-1硫酸溶液500mL.根據這兩種溶液的配制情況回答下列問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com