
| 6.72L |
| 22.4L/mol |
| 4.6g |
| 23g/mol |
| 6.72L |
| 22.4L/mol |
| 4.6g |
| 23g/mol |
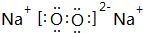 ,
, ;
;
| ||
| ||


 字詞句篇與同步作文達標系列答案
字詞句篇與同步作文達標系列答案科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 溫度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.250 | 0.012 |
| 容器 | 甲 | 乙 | 丙 | |
| 反應物投入量 | 1mol CO 2mol H2 | 1mol CH3OH | 2mol CH3OH | |
| 平衡數據 | CH3OH的濃度(mol/L) | c 1 | c 2 | c 3 |
| 反應的能量變化的絕對值(kJ) | a | b | c | |
| 體系壓強(Pa) | P1 | P2 | P3 | |
| 反應物轉化率 | α1 | α2 | α3 | |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 物質 名稱 | 丁烷與 2--甲基丙烷 | 紅磷 與白磷 | 庚烷與 十六烷 | 氕與 氘、氚 | 新戊烷與 2,2--二甲基丁烷 | 2--甲基戊烷與 2,3--二甲基丁烷 |
| 相互 關系 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、①② | B、②③ | C、③④ | D、②④ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 弱酸化學式 | CH3COOH | HCN | H2CO3 |
| 電離平衡常數(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7 K2=5.6×l0-11 |
| A、向醋酸溶液加水稀釋時,醋酸的電離平衡逆向移動 |
| B、等物質的量濃度的各溶液pH關系為:pH(NaCN)>pH(Na2CO3)>pH(CH3COONa) |
| C、a mol/L HCN溶液與b mol/L NaOH溶液等體積混合后,所得溶液中c(Na+)>c(CN-),則a一定大于b |
| D、同濃度CH3COONa和KCN溶液中c(Na+)-c(CH3COO-)小于的c(K+)-c(CN-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com